题目内容
【题目】某化学实验小组需制备O2并进行O2部分性质实验,结合以下装置,回答下列问题:
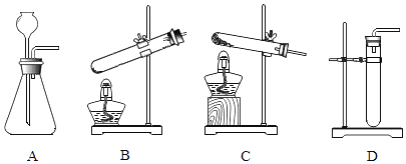
(1)甲同学利用KClO3和MnO2制备O2 , 其发生装置应选用上述装置中的________( 选填装置对应的字母),收集O2的方法是________(只填一种),可用________检验O2;
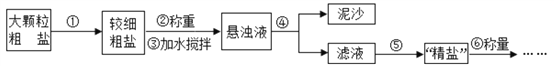
(2)乙同学提出可用H2O2和MnO2制备O2 , 本着废物利用的原则,可以从甲同学制备O2后剩余的固体中提取MnO2 , 则提取MnO2的操作步骤依次为:①溶解、②________、③洗涤、④干燥,其中步骤②比①多使用了一种玻璃仪器,该仪器名称是________,请写出乙同学制O2的化学方程式:________
(3)丙同学欲用少量的KMnO4和较多量的KClO3固体混合物加热,以较快制备较多量O2 , 你认为是否可行?________,(填“可行”或“不可行”),请说明理由:________;
(4)丁同学将硫粉置于收集到的O2中燃烧,可观察到发出________火焰(填火焰颜色),其产物的名称是________,它是形成酸雨的主要原因.
【答案】 C 向上排空气法 带火星的木条 过滤 漏斗 2H2O2![]() 2H2O+O2↑ 可行 KMnO4受热易分解,其分解后生成的二氧化锰又可以作为氯酸钾的催化剂,使氯酸钾快速分解 蓝紫色 二氧化硫
2H2O+O2↑ 可行 KMnO4受热易分解,其分解后生成的二氧化锰又可以作为氯酸钾的催化剂,使氯酸钾快速分解 蓝紫色 二氧化硫
【解析】(1)根据反应物的状态、反应条件、生成气体的密度及带火星的木条解答;(2)根据过滤需要漏斗解答;根据过氧化氢在二氧化锰的催化下分解生成水和氧气解答;(3)根据KMnO4受热易分解,其分解后生成的二氧化锰又可以作为氯酸钾的催化剂,使氯酸钾快速分解解答;(4)根据硫在氧气中燃烧生成二氧化硫并产生蓝紫色火焰解答。(1)KClO3和MnO2是固体,反应需要加热,且试管口需略向下倾斜,故选择C发生装置,由于氧气的密度比空气大,可选择向上排空气法收集,可用带火星的木条检验O2;(2)提取MnO2的操作步骤依次为:①溶解、②过滤、③洗涤、④干燥,其中步骤②比①多使用了一种玻璃仪器,该仪器名称是漏斗,请写出乙同学制O2的化学方程式为2H2O2![]() 2H2O+O2↑;(3)丙同学欲用少量的KMnO4和较多量的KClO3固体混合物加热,以较快制备较多量O2。方案可行。理由是KMnO4受热易分解,其分解后生成的二氧化锰又可以作为氯酸钾的催化剂,使氯酸钾快速分解;(4)丁同学将硫粉置于收集到的O2中燃烧,可观察到发出蓝紫色火焰,其产物的名称是二氧化硫,它是形成酸雨的主要原因。
2H2O+O2↑;(3)丙同学欲用少量的KMnO4和较多量的KClO3固体混合物加热,以较快制备较多量O2。方案可行。理由是KMnO4受热易分解,其分解后生成的二氧化锰又可以作为氯酸钾的催化剂,使氯酸钾快速分解;(4)丁同学将硫粉置于收集到的O2中燃烧,可观察到发出蓝紫色火焰,其产物的名称是二氧化硫,它是形成酸雨的主要原因。

 阅读快车系列答案
阅读快车系列答案