题目内容
【题目】某小组同学分别完成了图1所示的3个实验(图中a处连接压强传感器)。图2中的曲线1、2、3分别表示加入等体积相应液体后,烧瓶1、2、3内压强随时间的变化趋势。下列说法不正确的是
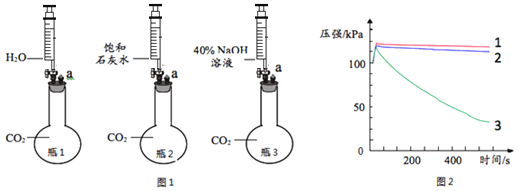
A. 对比曲线1和2可知,二氧化碳和水一定发生了化学反应
B. 由于注入液体压缩了瓶内的气体,所以三个实验的起始阶段压强都快速增大
C. 对比曲线1和3可知,二氧化碳和氢氧化钠一定发生了化学反应
D. 对比曲线2和3可知,40% NaOH溶液比饱和石灰水更适合吸收二氧化碳
【答案】A
【解析】
A、对比曲线1和2只能说明饱和石灰水和二氧化碳发生反应了,但并不能说明二氧化碳与水反应了,1中压强减小的原因也可能是二氧化碳溶于水产生的,选项错误;
B、在实验的开始阶段将三种不同的液体加入到盛有二氧化碳的烧瓶中,气体压强都快速增大是因为液体压缩了瓶中的气体使瓶内气压增大,选项正确;
C、对比曲线1和3,曲线3氧气明显减小,说明压强减小除了水的作用外,氢氧化钠也起了作用,从而说明了二氧化碳与氢氧化钠发生了化学反应,选项正确;
D、对比曲线2和3,曲线3压强减小明显,说明40% NaOH溶液比饱和石灰水吸收二氧化碳的能力强,更适合吸收二氧化碳,选项正确,故选A。

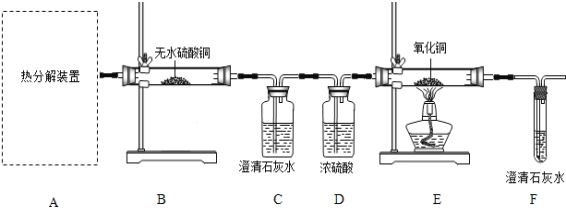
【题目】工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
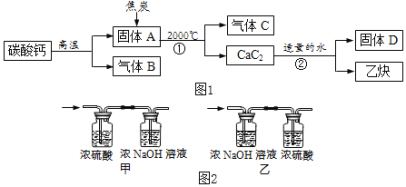
(资料)
(1)碳酸钙高温分解可得两种氧化物。
(2)浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
(讨论)(1)C、B组成元素相同,C有毒,反应①化学方程式为_________。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_________。
(测定乙炔组成)
资料:一个乙炔分子有四个原子构成。
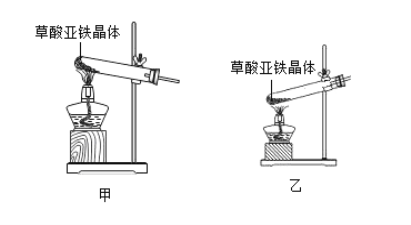
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
装置 | 反应前质量 | 反应后质量 |
浓硫酸 | 125.3g | 127.1g |
浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_________。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g
(6)乙炔的化学式为______________。