题目内容
【题目】柴油机尾气中的主要污染物是氮氧化物,某种尾气处理技术利用氨气与氮氧化物发生化学反应,降低污染物排放,反应的微观示意图如图:
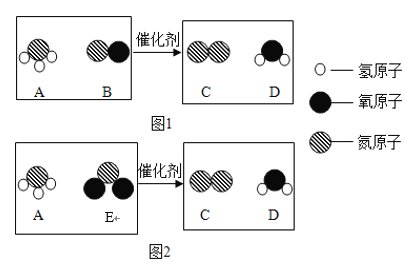
(1)一个A分子是由_____个原子构成的;B的化学式为_____。
(2)上述反应所涉及的物质中,属于氧化物的是_____(填字母序号)。
(3)反应图1涉及的含氮元素物质中,氮元素化合价最低的是_____(填字母序号)。
(4)反应图2的符号表达式为_____。
(5)上述反应中,一定发生改变的是_____(填字母序号)。
A.元素种类 B.分子种类 C.原子种类
(6)E和B的组成元素相同,E能与水反应而B不能,请从微观角度解释其化学性质不同的原因:_____。
【答案】A;NO;BDE;A;8NH3+6NO2![]() 7N2+12H2O;B;分子构成不同;
7N2+12H2O;B;分子构成不同;
【解析】
(1)由微粒的构成可知,一个A分子是由4个原子构成的;B的化学式为:NO;
(2)由微粒的构成可知,上述反应所涉及的物质中,B、D、E的分子由两种原子构成,其中一种原子只氧原子,属于氧化物;
(3)由微粒的构成可知,化合物中化合价代数和为0的原则,反应①涉及的含氮元素物质有A是NH3,氢元素的化合价为+1,设氮元素的化合价为X,x+1×3=0,则,x=-3价;、B是NO,氧元素的化合价为-2价,故氮元素的化合价为+2价、是N2中氮元素的化合价是0,故氮元素化合价最低的是A;
(4)由反应的微观示意图可知,反应②的符号表达式为:8NH3+6NO2![]() 7N2+12H2O;
7N2+12H2O;
(5)由微粒的变化可知,上述反应中,一定发生改变的是分子的种类;
(6)E和B的组成元素相同,E能与水反应而B不能,从微观角度分析其化学性质不同的原因:E和B两种物质的分子的构成不同。

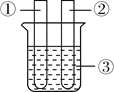
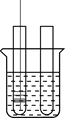
【题目】小李同学设计下表所示实验,探究金属铜对H2O2分解速率的影响.
操作 | 装置 | 现象 |
(1)取一个铜丝网,卷成筒形,固定在铁丝上. |
| |
(2)分别向①和②中注入15mL、30%的H2O2溶液,并放入盛有热水的③中。 |
| 约1min后可观察到①和②中都有少量气泡产生。 |
(3)把铜丝网(连同固定的铁丝)插入①中。 |
| ①中有大量气泡产生,5min后不再有气泡产生;此时②中仍然不断有少量气泡产生。 |
回答下列问题:
(1)仪器②中实验的目的是________。
(2)能否得出铜可以加快H2O2分解速率的结论________(填“是”或“否”)。
(3)如果用上述实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是________。
A.称量实验前铜丝网的质量和实验后干燥铜丝网的质量
B.向仪器②中加入二氧化锰
C.将实验后的铜丝网进行加热
D.将铁丝换成铜丝
E.将过氧化氢溶液加水稀释
(4)实验后确定铜可以加快H2O2分解的速率,请写出该反应的化学式表达式_______________。
【题目】小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
项目 | 实验操作 | 实验现象 | 实验结论或总结 | |
结论 | 总结 | |||
实验一 | 取5 mL 5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是____________________________ | 二氧化锰是过氧化氢分解的催化剂 |
实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | ________________________________________________________ | |
实验三 | ____________________________________________________________ | ________________________ | 二氧化锰能加快过氧化氢的分解 | |
(1)请你帮小丽同学填写上表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用:
__________________________________________________________________。
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
第一方面的实验操作中包含了两次称量,其目的是:__________________________________。称量前,要将天平调平衡,首先要把_______________,然后才调节平衡螺丝;称量粉末状固体时若药品量不足,此时一只手用药匙取药品移至天平左盘上方,另一只手应____________________,使少量药品落人盘中。
第二方面的实验是利用“实验三”反应后试管内的固体剩余物继续实验,其目的是:________________________________________。
(4)过氧化氢能被二氧化锰催化分解放出O2的符号表达式为:
_________________________________________________________。
【题目】鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究.
(1)将20mL溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算20ml溶质质量分数为35%的浓盐酸的质量为_____g;(溶质质量分数为35%的浓盐酸的密度ρ为1.2g/mL)
步骤2:计算所需加入水的体积为_____mL;
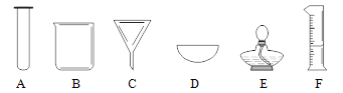
步骤3:根据计算结果,用_____分别量取所需的水和浓盐酸;
步骤4:先量取水倒入烧杯中,然后量取浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
(2)测得鸡蛋壳、空烧杯的质量后,将16g鸡蛋壳置于烧杯中,将配制的稀盐酸全部加入(盐酸过量),用玻璃棒充分搅拌,使其充分反应,直到不再产生气泡为止(假设鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录 如表:
鸡蛋壳的质量 | 空烧杯的质量 | 充分反应后,烧杯及内容物的总重量 |
16g | 60g | 155.6g |
①实验中生成二氧化碳的质量为_____g.
②计算该鸡蛋壳中碳酸钙的质量分数________.