题目内容
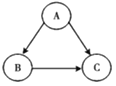
【题目】硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如下的流程图(部分反应物和生成物已省略).
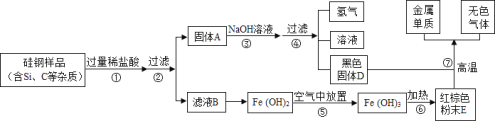
(查阅资料)常温下,单质硅不能与盐酸反应,但能与氢氧化钠溶液反应:Si+2NaOH+H2O═Na2SiO3+2H2↑
根据以上信息,回答下列问题:
(1)固体A的成分为_____,E的化学式为_____。
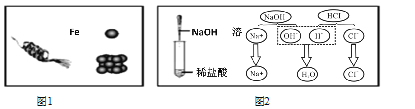
(2)滤液B中的阳离子有Fe2+和_________;步骤③中加入NaOH溶液的作用是_________;
(3)操作②中玻璃棒的作用是_____,若过滤速度太慢,原因可能是_____(写一点)
(4)若步骤⑤为化合反应,写出相关的化学方程式_____。步骤⑦属于_____基本反应类型。
【答案】Fe、C Fe2O3 H+ 与硅反应,验证硅钢中含硅 引流 滤纸没有紧贴漏斗内壁(合理即可) 4Fe(OH)2+O2+2H2O=4Fe(OH)3 置换反应
【解析】
(1)硅钢中的铁和盐酸反应会生成氯化亚铁和氢气,所以滤液B是氯化亚铁和盐酸的混合物,固体A中含有碳、硅,硅和氢氧化钠溶液反应会生成硅酸钠和氢气,所以黑色固体D是碳,氢氧化铁加热生成氧化铁和水,所以E是氧化铁,氧化铁和碳在高温的条件下生成铁和二氧化碳,经过验证,推导正确,所以固体A的成分为硅(或Si)和碳(C),E的化学式为Fe2O3;
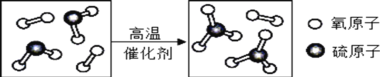
(2)二氧化碳和木炭在高温条件下生成一氧化碳;滤液B中的阳离子有Fe2+和过量的H+;步骤③中加入 NaOH溶液是为了除去固体A中的硅;
(3)过滤过程中玻璃棒的作用是引流,若过滤速度太慢,原因可能是滤纸没有紧贴漏斗内壁;
(4)步骤⑤中发生的是化合反应中,反应物是Fe(OH)2与氧气和水,生成物是氢氧化铁,化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;步骤⑦氧化铁和木炭反应生成铁和二氧化碳,属于置换反应。

【题目】下列“课外实验”得出的结论错误的是
选项 | A | B | C | D |
课外 实验 |
|
|
|
|
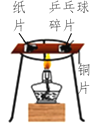
实验 结论 | 说明蜡烛 含有炭黑 | 说明有些花的色素 可做酸碱指示剂 | 不同物质着火点不同 | 说明同种溶质在不同种 溶剂里溶解性不同 |
A. AB. BC. CD. D