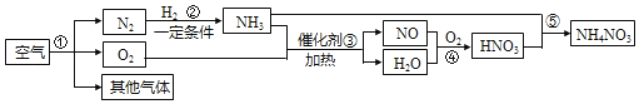
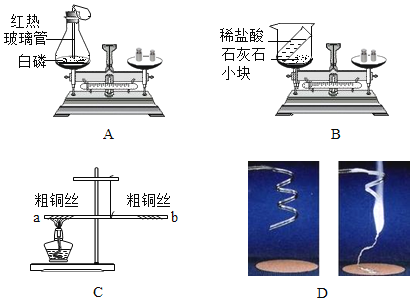
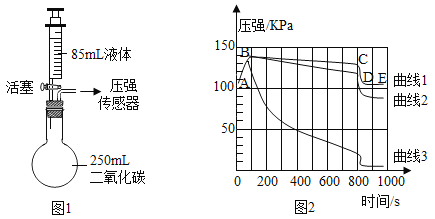
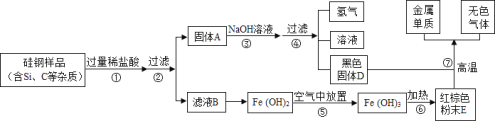
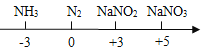��Ŀ����
����Ŀ������A��B��C��ת����ϵ(������Ϊһ�����з�Ӧ)��ͼ��ʾ��
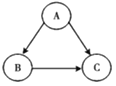
(1)��A��B��C���ǽ������ʣ��������������ǿ����______(����)��
(2)��A��B��CΪ��̼�����εݼ��Ļ����B��C�ֱ����ơ�þ���ơ�������Ԫ���е�һ�֣�����AΪ______����B��C����Ӧ�Ļ�ѧ����ʽΪ______��
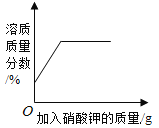
(3)��A��B��C�ֱ�ΪNaCl��NaNO3��Na2SO4������Һ�е�һ�֣���C��______��Һ����A��C����Ӧ�Ļ�ѧ����ʽΪ______(дһ��)��
���𰸡�A ������̼ Ba(OH)2+Na2CO3�TBaCO3��+2NaOH ������ Ba(NO3)2+Na2SO4�TBaSO4��+2NaNO3
��������
��1��A��ת��ΪB��C��λ��ǰ��Ľ����ܰ�����������Ľ�����������Һ���û��������������������ǿ����A��
��2����A��B��CΪ��̼�����εݼ��Ļ����B��C�ֱ����ơ�þ���ơ�������Ԫ���е�һ�֣�B��ת��ΪC����̼������ת��Ϊ̼�ᱵ��������̼��ת��Ϊ̼���ơ�̼��ƣ���ΪB��ת��ΪC��A��B��CΪ��̼�����εݼ��Ļ����������AΪ������̼��BΪ̼���ƣ�CΪ̼�ᱵ��������̼��ơ�̼��þ����Ϊ���ǵ���Է�������С��̼���ƣ���B��C����̼����������������Һ��Ӧ����̼�ᱵ�������������ƣ���Ӧ�Ļ�ѧ����ʽΪ��Ba��OH��2+Na2CO3�TBaCO3��+2NaOH��
��3����A��B��C�ֱ�ΪNaCl��NaNO3��Na2SO4������Һ�е�һ�֣������������Ȼ�����Һ��Ӧ�������ᱵ��ɫ�������Ȼ��ƣ��������ᱵ��Һ��Ӧ�������ᱵ�����������ƣ��Ȼ���������������Һ��Ӧ�����Ȼ��������������ƣ���C����������Һ��A��C���������������ᱵ��Һ��Ӧ�������ᱵ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪ��Ba��NO3��2+Na2SO4�TBaSO4��+2NaNO3��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ѧ��ȤС��̽������������ʱ����һ��ȥ������Ĥ��þ��������һ������ϡ�����У������ݲ�������ַ�Ӧ���ã������Թ����лҰ�ɫ������д���������ݵķ�Ӧ��ѧ����ʽ______��
��������⣩�Ұ�ɫ������ʲô���ʣ�
��������裩��С����Ϊ�Ұ�ɫ����Ϊ̼��þ��MgCO3��������ͬѧ��Ϊ����Ҫʵ����ܷ�С���IJ��룬������_____________________��
��С����Ϊ���ڷ�Ӧ���Ȼ�þ��������ƫ�࣬�Ұ�ɫ����Ϊ�������ܽ���Ȼ�þ���塣
��Сͮ��Ϊ�Ұ�ɫ����Ϊ__________________��
��ʵ��̽��1��
ʵ����� | ���� | ���� |
��ȡ�Թ��е��ϲ���Һ�������������Ȼ�þ���� | �Ȼ�þ����__��ѡ�����ܽ����������ܽ����� | С�������� |
��ȡ������ɫ������������ϡ������ | û������ð�� | Сͮ������� |
��������̽���������ԭ�в������˷�
���������ϣ�
HCl+AgNO3�THNO3+AgCl����AgCl��һ�ְ�ɫ�������Ȼ������������壬��ʹ��ɫʯ����ֽ��졣����
��ʵ��̽��2��
��������ȡ�Ұ�ɫ���������Թ��м��ȣ���պ����������Һ�IJ����������Թ��ڣ��������ϵ���Һ���ְ�ɫ���ǣ�֤��������__���塣��μ�����������_______��ʵ�鲽�衢�����ۣ���
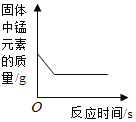
ͬѧ�������ʦ���֪��������þ��ϡ���ᷴӦʱ����Һ�ᾭ�������Ե������Ҽ�������ǿ�Ĺ��̣��Ӷ������˼�ʽ�Ȼ�þ�������������ܣ���ʽ�Ȼ�þ���ڶ�����ɽṹ����ѧͨʽ�ɱ�ʾΪMgx��OH��yClzmH2O������2x��y��z=0��0��m��6����
����˼��չ��
��1����þ��ϡ���ᷴӦ��ʵ��ʱ��Ϊ�˲����Թ��г��ֻҰ�ɫ������þ��������_______��
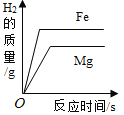
��2����Ƭ��ͭƬ����ϡ�����в���������Ҳ����ͬ���ݴ��Ʋ�����Ļ�Ա�ͭ_____��
����Ŀ�������ڽ�ͨ���������Ź㷺��Ӧ�ã�����������Ϣ�ش����⡣
Ӧ�� |
|
|
�������� |
�õ��IJ��� | ��̥���� | ��������﮺Ͻ� | �������� |
(1)������ͨ�����õ��IJ������ڽ������ϵ���______(��һ�ּ���)�������л��ϳɲ��ϵ���______��
(2)��ɻ�C919����ʹ�úϽ���ϣ�ԭ����______��������������Ŀ�������ۣ�������������ã���ҵ�ϳ���ϡ������������(Fe2O3)���÷�Ӧ�Ļ�ѧ����ʽ��______��
(3)��ʯȼ�ϵĴ���ʹ�ã������˻�������Ⱦ����Դ�Ŀݽߵ����⣬���������ڹ㷺�ƹ�ʹ���Ҵ����ͣ���ô���______��