题目内容
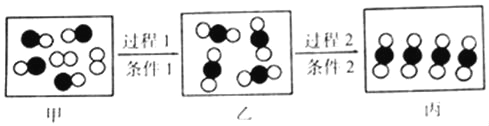
【题目】实验室制取氧气并进行相关实验。
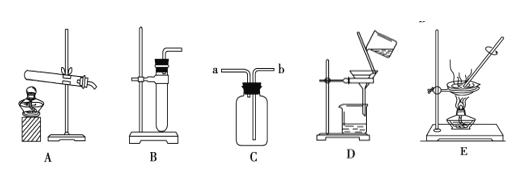
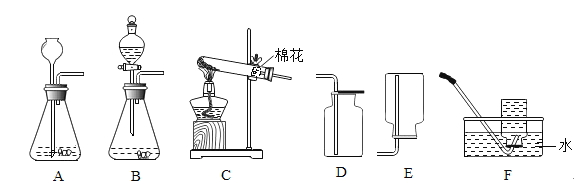
①双氧水和二氧化锰制氧气的化学方程式是_______________________。取用二氧化锰操作正确的是___________(选填编号)。

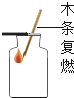
②探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如下:
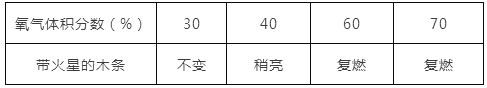
根据上述实验数据得出的结论是___________________________。
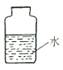
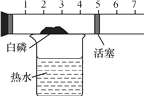
在集气瓶中注入占其容器50%的水(如图所示),用排水法收集氧气,将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,推测实验现象并说明理由。_________________
③双氧水分解也可用氧化铜作催化剂。在0.5g氧化铜中滴加双氧水,反应结束后固体仍为0.5g且呈_______色。
设计一个实验,证明在双氧水分解反应后,氧化铜化学性质没有发生改变。
步骤 | 现象 | 结论 |
______________ | _______________ | 氧化铜化学性质没有改变 |
【答案】2H2O2![]() 2H2O+O2↑c能使带火星的小木条复燃的不一定是纯氧带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度黑将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2ml过氧化氢溶液试管中有大量气泡冒出,且能使带火星的木条复燃
2H2O+O2↑c能使带火星的小木条复燃的不一定是纯氧带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度黑将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2ml过氧化氢溶液试管中有大量气泡冒出,且能使带火星的木条复燃
【解析】
①根据反应的原理来书写化学方程式,根据粉末状药品的取用方法来分析;②根据表格数据以及实验现象来分析;③根据催化剂的性质以及物质的颜色来分析。
①过氧化氢在二氧化锰的催化作用下分解为水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;二氧化锰是粉末状药品,取用时,用药匙取二氧化锰,将试管横放,用药匙将二氧化锰送至试管底部;
2H2O+O2↑;二氧化锰是粉末状药品,取用时,用药匙取二氧化锰,将试管横放,用药匙将二氧化锰送至试管底部;
②根据表格中反应的信息可知:氧气的体积分数达到60%时能使带火星的木条复燃,所以能使带火星的木条复燃不一定是纯净的氧气;在集气瓶中注入占其容器50%的水,用排水法收集氧气,将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,可能会观察到带火星的木条复燃,这是因为氧气的浓度达到了使其复燃的纯度;
③氧化铜在该反应中是催化剂,其质量与化学性质在反应前后不变,在0.5g氧化铜中滴加双氧水,反应结束后固体仍为0.5g且呈黑色;催化剂反应前后化学性质不变,将反应后的混合物过滤,向盛有该滤渣的试管中重新加入2mL过氧化氢溶液后,试管中有大量气泡冒出,且能使带火星的木条复燃;得出结论:氧化铜的化学性质在化学反应前后没有发生改变。

【题目】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰.该小组同学进行如下探究:

(1)探究一:铁丝在氧气中燃烧为什么会火星四射?
下表是小组同学将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
请你分析并回答:写出铁丝在氧气中燃烧的化学表达式:_____,铁燃烧时的“火星四射”现象可能与_____有关,表中未填的一项你估计应当是________。
(2)探究二:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入火焰,导出其中物质,在另一端管口点燃,也有火焰产生.由此可知:蜡烛燃烧产生的火焰是由________(填“固态”或“气态”)物质燃烧构成的。
(3)探究三:物质燃烧产生火焰的根本原因是什么?
查阅资料
物质 | 熔点/℃ | 沸点/℃ | 燃烧时温度/℃ |
石蜡 | 50~70 | 300~550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由表中数据可知:物质燃烧能否产生火焰与其________(填“熔点”或“沸点”)和燃烧时温度有关,由此推测:钠在燃烧时,________(填“有”或“没有”)火焰产生。