题目内容
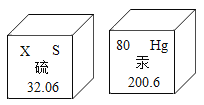
【题目】根据下图①氟元素、②钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
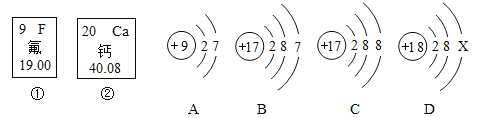
请你回答:
(1)氟元素的相对原子质量为______,钙元素的原子序数为______。
(2)D表示原子,则X=______,它的化学性质_________(填“稳定”或“不稳定”)。
(3)A、B、C、D属于同种元素的粒子是______(填标号)。
(4)B粒子的化学性质与A、C、D中哪一种粒子的化学性质相似______(填标号)。
(5)元素周期表是我们学习化学和研究化学的重要工具。下表是元素周期表中1~18号元素原子核外电子排布,请你对它进行研究:
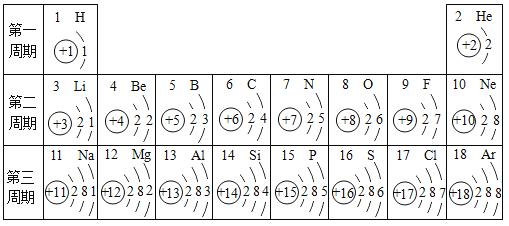
①12号元素名称是____,它属于____元素(填“金属”或“非金属”),它在化学反应中容易_____电子(填“得到”或“失去”),形成_________ (填粒子符号)。它和17号元素形成的化合物的化学式为_______。
②从上表中你可得到什么规律:__________。
【答案】19.00 20 8 稳定 BC A 镁 金属 失去 Mg2+ MgCl2 同一周期(或同一横行),从左到右各元素原子核电荷数依次递增;同一周期,各元素原子的电子层数相同;同一族(或同一纵行)各元素原子的最外层电子数相同(氦除外)。(合理即可)
【解析】
(1)元素周期表信息示意图中元素名称正下方表示的是该元素的相对原子质量,左上角表示的是该元素的原子序数,根据图①,氟元素的相对原子质量为:19.00,根据图②钙元素的原子序数为:20。
(2)D表示原子,从原子结构示意图中可知,该原子核电荷数为18,根据原子中质子数=核外电子数,18=2+8+X,则X=8,最外层电子数是8的电子层结构是相对稳定结构,因此它的化学性质稳定。
(3)质子数相同的原子(或简单离子即带电的原子)属于同一种元素。A、B、C、D中B、C两种粒子质子数相同,因此属于同种元素的粒子是:BC。
(4)最外层电子数相同的原子化学性质相似,B原子的最外层电子数为7,A原子的最外层电子数也为7,因此B粒子的化学性质与A、C、D中化学性质相似的是:A。
(5)①12号元素名称是:镁;根据元素名称的偏旁是“钅”,它属于金属元素;从镁原子的结构示意图中可知,镁原子最外层只有2个电子,少于4个,在化学反应中容易失去电子,一个镁原子失去2个电子,带2个单位正电荷,因此形成的镁离子符号为:Mg2+。17号元素是氯元素,氯原子最外层有7个电子,在化学反应中易得到一个电子,形成带一个单位负电荷的氯离子,氯离子带一个单位负电荷,显-1价,而一个镁离子带二个单位正电荷,显+2价,根据化合物中元素化合价的代数和为零,镁元素和氯元素形成的化合物的化学式为MgCl2。
②分析元素周期表中1~18号元素原子核外电子排布,从表中可以得到的规律有:同一周期(或同一横行),从左到右各元素原子核电荷数依次递增;同一周期,各元素原子的电子层数相同;同一族(或同一纵行)各元素原子的最外层电子数相同(氦除外)。(合理即可)