题目内容
(6分) 化学小组进行实验探究,请你参与研究。
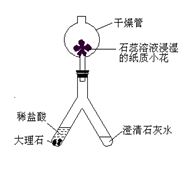
(1)利用右图所示装置进行二氧化碳的制备和性质实验。实验进行一段时间后,“人”字管左端发生反应制备二氧化碳;右端可以观察到的现象是 ;被石蕊溶液浸湿的纸质小花的颜色变为红色的原因是 ;若将燃烧的木条从干燥管的上管口伸入管内,可以看到燃烧的木条熄灭,以上实验说明二氧化碳具有 点性质。
(2)在探究CO2和NaOH是否发生反应时,设计出下图所示的三种装置进行实验,请回答问题:
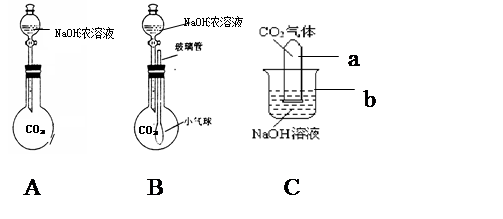
① 以上三个实验中,B、C两个实验有明显现象,请你记录观察到的实验现象:
实验B: ; 实验C: 。
② 实验A因选用的仪器不当导致未能观察到明显现象,请你寻找一种物品替代该装置中的烧瓶,使实验获得成功,你将选用的物品是 。
(1)利用右图所示装置进行二氧化碳的制备和性质实验。实验进行一段时间后,“人”字管左端发生反应制备二氧化碳;右端可以观察到的现象是 ;被石蕊溶液浸湿的纸质小花的颜色变为红色的原因是 ;若将燃烧的木条从干燥管的上管口伸入管内,可以看到燃烧的木条熄灭,以上实验说明二氧化碳具有 点性质。

(2)在探究CO2和NaOH是否发生反应时,设计出下图所示的三种装置进行实验,请回答问题:

① 以上三个实验中,B、C两个实验有明显现象,请你记录观察到的实验现象:
实验B: ; 实验C: 。
② 实验A因选用的仪器不当导致未能观察到明显现象,请你寻找一种物品替代该装置中的烧瓶,使实验获得成功,你将选用的物品是 。
(1)澄清的石灰水变浑浊
二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液变红色 三
(2)①B中氢氧化钠滴入后,气球逐渐胀大 C试管内液面逐渐上升
②用软塑料瓶代替烧瓶
二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液变红色 三
(2)①B中氢氧化钠滴入后,气球逐渐胀大 C试管内液面逐渐上升
②用软塑料瓶代替烧瓶
试题分析:(1)根据二氧化碳的三点性质分析,能与石灰水反应生成碳酸钙沉淀,使石灰水变浑浊;能溶于水,所得溶液中含碳酸呈酸性,可使酸碱指示剂变色;不可燃也不支持燃烧,能使燃烧的木条熄灭。
(2)二氧化碳能与氢氧化钠反应,使二氧化碳气体被消耗,使烧瓶内和试管内压强降低,外界大气压比内部气压大,故①B中氢氧化钠滴入后,气球逐渐胀大; C试管内液面逐渐上升。
②二氧化碳与氢氧化钠反应本无明显现象,而二氧化碳消耗会使体系压强降低,BC就是使用了该原理,要使A也能有明显现象,可使用可自由改变形状的反应容器,如软塑料瓶。
点评:本题是对二氧化碳的化学性质的考查,以及对实验装置的改进,该题对学生灵活运用知识解题的要求较高。

练习册系列答案
相关题目






 CaCO3+CO2↑
CaCO3+CO2↑