��Ŀ����
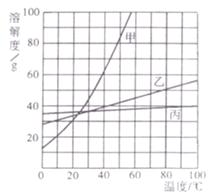
����Ŀ������̽��һ�ֹ�������A�ijɷ֣���֪���п��ܺ���NH4NO3��MgO��BaCl2��Na2SO4���������е����ֻ���֣���ͼ��ʾ����ʵ�飬���ֵ�������ͼ������������������з����ķ�Ӧ��ǡ����ȫ��Ӧ����
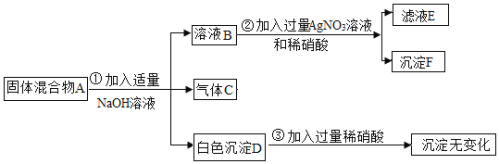
��1������C����ζΪ______������������ˮ��������Һ______7��������������С������������֮һ����
��2����ҺE�е�������______�֣�����F�Ļ�ѧʽΪ______��
��3���ù���������һ�����ڵ���______��д��ѧʽ����
��4����ҺB�д��ڵ��������Ϊ______��д���ӷ��ţ���
��5��д�����̢������ɳ���D�Ļ�ѧ����ʽ______��
���𰸡��̼�����ζ ���� 3 AgCl NH4NO3��BaCl2��Na2SO4 NO3-��Cl- BaCl2+Na2SO4=2NaCl+BaSO4��
��������
�⣺�������������ܹ��������壬���֪ԭ������к���笠�������C�ǰ��������ܹ����ɲ���������İ�ɫ�������ʽ��A�п��ܺ��е��������������֪�ó��������ᱵ���������к��������ƺ��Ȼ�������ҺB������������ϡ��������ɳ���F��F���Ȼ����������ͼ�ƶϺ�����
��1���ɷ���֪C�ǰ������������д̼�����ζ��������ˮ��Һ�ʼ��ԣ�pH����7��
��2������A�к���NH4NO3��BaCl2��Na2SO4��B�Ǻ��������Ʒ�Ӧ�����Һ����B�������ơ��Ȼ��ƣ�����Һ����������Ӧ������ϡ���ᣬ��E�к���ϡ���ᡢ�����Ƽ��������������������ʣ�����F��AgCl��
��3���ɷ���֪�û�����к���NH4NO3��BaCl2��Na2SO4��
��4����ҺB�д��������ơ��Ȼ��ƣ����������ΪNO3-��Cl-��
��5�������������ɳ���D�ķ���ʽΪ��BaCl2+Na2SO4=2NaCl+BaSO4����
�ʴ�Ϊ����1���̼�����ζ�����ڣ���2��3��AgCl��
��3��NH4NO3��BaCl2��Na2SO4��
��4��NO3-��Cl-��
��5��BaCl2+Na2SO4=2NaCl+BaSO4����

����Ŀ��С����һֻ����������п�Ͻ𣩣�������ʵ��̽�����������ĺ��������õ��ӳӳƵ������������� 25.00�ˣ�����ϡ����ֶ�����������ַ�Ӧ��ʵ���������±���
��1�� | ��2�� | ��3�� | ��4�� | ��5�� | |
����ϡ������������ˣ� | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 |
��ַ�Ӧ��ʣ�������������ˣ� | 24.35 | 23.70 | 23.05 | 23.00 | 23.00 |
�����ϱ������ݷ���������������⣺
��1������������������_____�ˡ�
��2������ϡ���������ʵ����������Ƕ��٣���д��������̣�________
��3����4�μ��������ַ�Ӧ����Һ�е�������_____���ѧʽ����