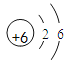题目内容
【题目】将一种无色无味的液体A装入试管,用带火星的木条试验,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C、瓶底有少量液体D的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F。
(1)写出它们的化学式A:______ F:______
(2)黑色粉末B在A的分解反应中起催化作用,写出该反应的化学方程式___________
【答案】H2O2; Fe3O4 2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
【解析】
由于C气体能使带火星的木条复燃,可以判断为氧气,而过氧化氢在黑色固体二氧化锰的催化作用下能快速生成氧气,可以判断A为过氧化氢,B为二氧化锰,铁丝在氧气中燃烧火星四射,生成黑色固体四氧化三铁,可以判断E为铁,F为四氧化三铁。
(1)A为过氧化氢,化学式为H2O2;F为四氧化三铁化学式为Fe3O4;
(2)B是二氧化锰,A是过氧化氢,该反应的化学方程式为:2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。

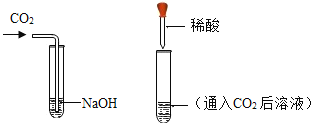
【题目】化学课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象,CO2和NaOH是否确实发生了化学反应?
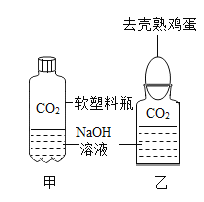
(1)我设计了甲、乙两个实验来验证,如图所示,实验现象为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”。小虎同学认为上述实验是可行的,其共同原理是:_________。小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:______________。我思考后,又补充了一个实验来回答,这个实验是:_________。
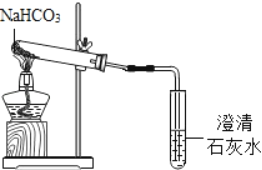
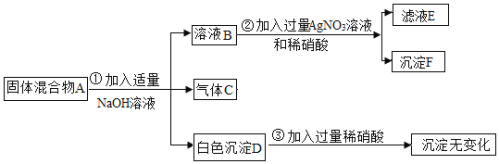
(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
实验步骤和方法 | 实验现象 | 实验结论 | |
方案一 |
| ________ | 二氧化碳和氢氧化钠发生了化学反应 |
方案二 | ________ | ________ |
写出方案2中所涉及的化学方程式________________。
(3)由此探究,我得到的启示是:________________。