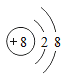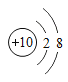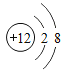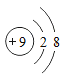题目内容
【题目】将Cu-Zn合金样品20g放入足量稀硫酸中,所产生氢气的质量与反应时间的关系如图所示.试计算:
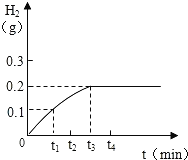
(1)反应产生氢气的质量为______g
(2)原样品中所含锌的质量分数_____.
(3)实验测得20g该样品与154.7g某稀硫酸恰好完全反应,求此时所得溶质的质量_____
【答案】0.2 32.5% 16.1g
【解析】
(1)由图可知,反应后生成氢气的质量为0.2g,故填0.2。
解:设参加反应的锌的质量为x,生成硫酸锌的质量为y
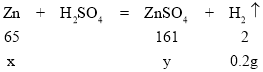
65:2=x:0.2g x=6.5g
161:2=y:0.2g y=16.1g
原样品中所含锌的质量分数为![]() ×100%=32.5%
×100%=32.5%
答:(2)原样品中所含锌的质量分数为32.5%;
(3)反应后所得溶质硫酸锌的质量为16.1g。

【题目】实验室常用高锰酸钾制取氧气,可能用到的装置如图所示。
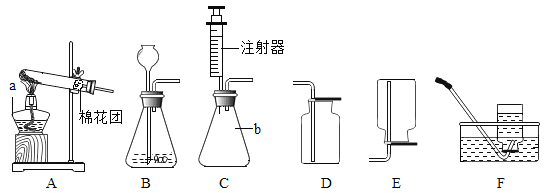
(1)本实验可选用的发生和收集装置为________(填字母)。
(2)取一定量的高锰酸钾固体,充分加热,发现实际产生氧气量远高于理论值,则可能的原因有________(测定过程中产生的误差可忽略)。
(3)某同学进行该实验并用排水法收集O2.下列操作正确的是__(填字母)
A 未检查装置气密性即向大试管中加入高锰酸钾固体
B 当导管口有连续气泡均匀冒出时,开始收集氧气
C 集气瓶中氧气收集满后,先用玻璃片盖住集气瓶口,再将其移出水面
D 气体收集完毕后,先熄灭酒精灯,再将导管移出水面
(4)实验室也可用双氧水制氧气。某同学为研究MnO2粉末用量对双氧水分解速率的影响,做了以下实验:采用不同质量的MnO2粉末做催化剂,每次均用30mL 10%的双氧水(其他实验条件均相同),测定收集500mL氧气所用的时间,结果如表:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
MnO2用量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 |
所用时间/s | 17 | 8 | 6 | 3 | 2 | 2 | 2 | 2 | 2 |
①写出上述反应的符号表达式: ________,该反应的基本类型是__________。
②该实验可得出的结论是______________。
③若上述实验选用B做发生装置,也可以制取氧气则长颈漏斗下端管口必须浸没在液体中,原因是_______。若选用C做发生装置,你认为选用装置C的优点是____________。
④在实验中也可以将注射器连接到装置B的导管口处,用来_________。
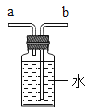
(5)实验室需少量甲烷气体,可用加热无水醋酸钠与碱石灰两种固体混合物制得。制甲烷气体的发生装置应选用________(填字母)装置,收集甲烷气可选用E或F装置,由此推断甲烷气具有的物理性质是_____________,若用如图装置收集该甲烷,气体由______端通入(填“a”或“b”)
(6)在实验室里制取氧气,既可采用分解过氧化氢的方法,也可采用分解氯酸钾的方法。上述两种方法的主要共同点有___________。
①采用MnO2均可改变其反应速率 ②反应都不需加热
③都利用含氧物质的分解来达到目的 ④两种方法所需仪器相同。
A ①③ B ③ ④ C ①② D ②④
(7)某同学在学习了MnO2对H2O2的分解的催化作用之后,对催化剂产生了浓厚的兴趣。于是,他设计下表所示实验,探究金属铜对H2O2分解速率的影响。
操 作 | 装 置 | 现 象 |
1.取一个铜丝网,卷成筒形,固定在铁丝上。 |
| |
2.分别向①和②中注入15mL、30%的H2O2溶液,并放入盛有热水的③中。 |
| 约1min后可观察到①和②中都有少量气泡产生。 |
3.把铜丝网插入①中。 |
| ①中有大量气泡产生,5min后不再有气泡产生;此时②中仍然不断有少量气泡产生。 |
回答下列问题:
(a)仪器②在实验中的目的是_____________
(b)能否可以得出铜可以加快H2O2分解的速率_______(填“是”或“否”)理由是_______。
(c)如果用上述实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是_____。
A 称量实验前铜丝网的质量并将实验后的铜丝网干燥称重
B 向仪器②中加入二氧化锰
C 将实验后的铜丝网插入AgNO3溶液中(已知铜可以和AgNO3溶液反应生成银白色固体)
D 将铁丝换成铜丝
E 将过氧化氢溶液稀释
(d)该同学查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是___________。
A MnO2只能作过氧化氢溶液分解的催化剂
B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率
D 用作催化剂的物质不可能是其他反应的反应物或生成物
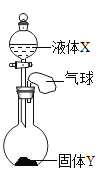
【题目】如图所示,将少量液体X加入烧瓶中,观察到气球逐渐膨胀。下表中液体X和固体Y的组合,符合题意的是( )
① | ② | ③ | ④ | |
| 过氧化氢溶液 | 水 | 水 | 水 |
| 二氧化锰 | 氯化钠 | 氢氧化钠 | 硝酸铵 |
A. ①②B. ①③C. ①③④D. ②③④
【题目】空气中氧气含量测定的再认识。
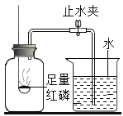
(实验回顾)如图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的化学式方程式:______________。
(2)实验原理:由于红磷燃烧消耗空气中的氧气使瓶内气体___________减小,烧杯中水倒吸到集气瓶中。若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
(问题提出)有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测量结果与理论值误差较大。
(实验改进)
Ⅰ根据铁在空气中生锈的原理,设计如图实验装置,再次测定空气中氧气含量。

(说明:装置中饱和食盐水、活性炭会加速铁生锈。)
II.测得实验数据如下表。
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
(交流表达)
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],化学方程式为______,计算氢氧化亚铁[Fe(OH)2]的相对分子质量Mr [Fe(OH)2] =_______。
(2)根据上表数据进行计算,改进实验后测得的空气中氧气的体积分数是______(计算结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:①______;②______。