题目内容
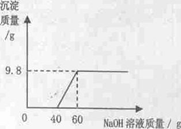
(12分)元明粉是重要的化工原料,右图是某品牌元明粉包装袋上的部分标签。
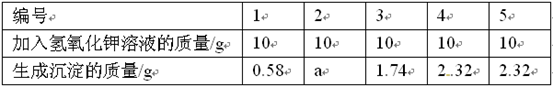
为测定该元明粉中Na2SO4含量是否符合标签要求,把15.0 g样品(假设只含不溶性杂质)
加入一定量的水溶解,过滤得100.0 g滤液。取10.0 g滤液,加入10%的BaCl2溶液20.8
g,恰好完全反应,反应的化学方程式:Na2SO4 + BaCl2 = 2NaCl + BaSO4↓。
(1)计算10.0 g滤液中Na2SO4的质量。
(2)根据这一次检测,计算并判断样品Na2SO4的含量是否符合标签要求。

为测定该元明粉中Na2SO4含量是否符合标签要求,把15.0 g样品(假设只含不溶性杂质)
加入一定量的水溶解,过滤得100.0 g滤液。取10.0 g滤液,加入10%的BaCl2溶液20.8
g,恰好完全反应,反应的化学方程式:Na2SO4 + BaCl2 = 2NaCl + BaSO4↓。
(1)计算10.0 g滤液中Na2SO4的质量。
(2)根据这一次检测,计算并判断样品Na2SO4的含量是否符合标签要求。

(12分)解:(1)设10.0 g滤液中Na2SO4的质量为m
Na2SO4 + BaCl2 = 2NaCl + BaSO4↓
142 208
m 10%×20.8 g

m="1.42" g (7分)
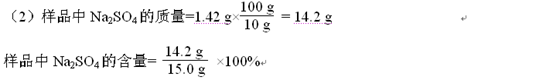 ≈94.7%
≈94.7%
因为94.7%<99%,不符合标签要求 (3分)
答:(1)10.0 g滤液中Na2SO4的质量为14.2 g。
(2)样品中Na2SO4的含量不符合标签要求。
假设、答正确、单位正确 (2分)
Na2SO4 + BaCl2 = 2NaCl + BaSO4↓
142 208
m 10%×20.8 g

m="1.42" g (7分)
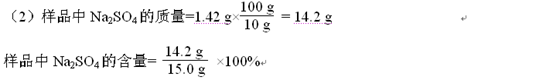 ≈94.7%
≈94.7% 因为94.7%<99%,不符合标签要求 (3分)
答:(1)10.0 g滤液中Na2SO4的质量为14.2 g。
(2)样品中Na2SO4的含量不符合标签要求。
假设、答正确、单位正确 (2分)
分析:(1)根据氯化钡溶液的质量和溶质质量分数求得氯化钡溶质的质量;再根据反应方程式即可求得反应的硫酸钠的质量;
(2)根据10g滤液反应的硫酸钠的质量即可求得100g滤液反应掉硫酸钠的质量;再根据硫酸钠的质量分数= ×100%即可求得样品中硫酸钠的质量分数,最后与标签中硫酸钠的质量分数比较即可判定是否符合标签要求.
×100%即可求得样品中硫酸钠的质量分数,最后与标签中硫酸钠的质量分数比较即可判定是否符合标签要求.
解:(1)设10.0 g滤液中Na2SO4的质量为m
Na2SO4 + BaCl2 = 2NaCl + BaSO4↓
142 208
m 10%×20.8 g

m=1.42g
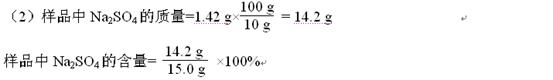 ≈94.7%
≈94.7%
因为94.7%<99%,不符合标签要求
答:(1)10.0g滤液中Na2SO4的质量为1.42g;(2)样品中Na2SO4的含量不符合标签要求.
点评:根据反应的化学方程式可以表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.
(2)根据10g滤液反应的硫酸钠的质量即可求得100g滤液反应掉硫酸钠的质量;再根据硫酸钠的质量分数=
 ×100%即可求得样品中硫酸钠的质量分数,最后与标签中硫酸钠的质量分数比较即可判定是否符合标签要求.
×100%即可求得样品中硫酸钠的质量分数,最后与标签中硫酸钠的质量分数比较即可判定是否符合标签要求.解:(1)设10.0 g滤液中Na2SO4的质量为m
Na2SO4 + BaCl2 = 2NaCl + BaSO4↓
142 208
m 10%×20.8 g

m=1.42g
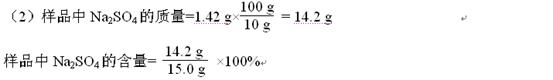 ≈94.7%
≈94.7% 因为94.7%<99%,不符合标签要求
答:(1)10.0g滤液中Na2SO4的质量为1.42g;(2)样品中Na2SO4的含量不符合标签要求.
点评:根据反应的化学方程式可以表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目