题目内容
【题目】(1)用化学符号填空:
①1个氧原子_____;②氯酸钾中氯的化合价_____;
③2个铁离子_____;④地壳含量最多的金属元素的氧化物_____.
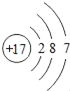
(2)如图是某元素的原子结构示意图,该原子核外有_____个电子层,在化学反应中容易_____电子(填“得”或“失”),所形成微粒的符号是_____,该微粒与铜离子形成化合物的化学式为_____.
【答案】(1) ① O ②+5 ③2Fe3+ ④Al2O3
(2)3 得 Cl_ CuCl2
【解析】
试题(1)①原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以一个氧原子,就可表示为 O;②氯酸钾的化学式为KClO3,钾元素显+1价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则x=+5价;③离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个铁离子可表示为:2Fe3+;④地壳中含量最多的金属元素是铝,氧化物还需要有氧元素,所以化学式是Al2O3.
(2)在原子结构示意图中圆圈内的数字为质子数,可知该元素原子核内有17个质子,最外层电子数为7,该元素的原子在化学反应中一般要得到1个电子而形成稳定结构,所以该元素的离子带负电荷,属于阴离子.该微粒与铜离子形成化合物的化学式为CuCl2.

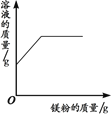
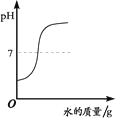
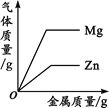
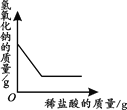
【题目】下列四个图像中,能正确反映对应变化关系的是( )
|
|
|
|
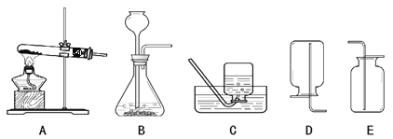
A.向一定量的稀盐酸中加入过量的镁粉 | B.向一定量的稀盐 | C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | D.向一定量氢氧化钠溶液中滴加稀盐酸 |
A. AB. BC. CD. D
【题目】镁的课堂,“镁”的享受。
资料①:镁可以在氮气、二氧化碳中燃烧;镁也能与水反应。
资料②:常温下,各物质开始沉淀的pH如下表:
物质 | 氢氧化铁 | 氢氧化铝 | 氢氧化镁 |
开始沉淀的pH | 1.5 | 3.3 | 9.4 |
Ⅰ.识镁
(1)镁元素的相关信息“ ”,画出镁原子的结构示意图:______。
”,画出镁原子的结构示意图:______。
Ⅱ.寻镁
用矿石(含MgO、Fe2O3、Al2O3和SiO2)制备氢氧化镁的流程示意图如下:
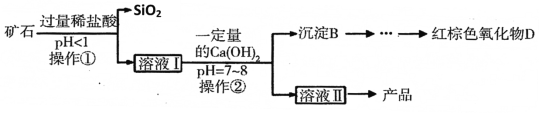
(2)从该流程推测SiO2具有的化学性质是______(写一条)。
(3)操作①中盐酸与Fe2O3反应的化学方程式为______。
(4)实验室完成操作②所用玻璃棒的作用是______。
(5)溶液Ⅰ中的阳离子有______种。
(6)沉淀B的成分有 ______ 。
Ⅲ.炼镁
(7)工业上用电解融熔氯化镁制取镁,可用来冷却镁蒸气的气体可以是______。
Ⅳ.用镁
(8)镁合金广泛用于携带式的器械和汽车行业中,达到轻量化的目的,主要利用其性质是______(写一点)。
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下图所示:
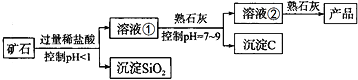
资料信息:部分金属阳离子以氢氧化物形成沉淀时溶液的pH如下表所示:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
根据以上信息进行分析,下列说法中错误的是
A. 加入稀盐酸时一定发生了复分解反应B. 沉淀C一定属于混合物
C. 上图所示制备氢氧化镁的流程中三次用到了过滤操作D. 溶液②中的溶质最多为2种