��Ŀ����
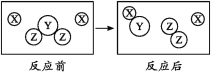
����Ŀ��������þ��һ����Ҫ�Ļ���ԭ�ϣ�ij��ʯ��MgO��Fe2O3��CuO��SiO2��ɡ������Ʊ�������þ������ʾ��ͼ����ͼ��ʾ��
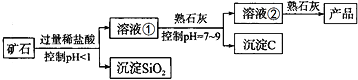
������Ϣ�����ֽ��������������������γɳ���ʱ��Һ��pH���±���ʾ��
������ | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
��ʼ���� | 1.9 | 4.2 | 9.1 |
��ȫ���� | 3.2 | 6.7 | 11.1 |
����������Ϣ���з���������˵���д������
A. ����ϡ����ʱһ�������˸��ֽⷴӦB. ����Cһ�����ڻ����
C. ��ͼ��ʾ�Ʊ�������þ�������������õ��˹��˲���D. ��Һ���е��������Ϊ2��
���𰸡�D
��������
A. ����ϡ����ʱ��������þ��������������ͭ��������Ӧ���Ҷ��ǽ������������������κ�ˮ�ķ�Ӧ���Ǹ��ֽ⣬����һ�������˸��ֽⷴӦ��˵����ȷ��
B. ����C���ڿ���pH��7��9֮�䣬������ʯ�����Ȼ������Ȼ�ͭ����������������������ͭ����������һ�����ڻ���˵����ȷ��
C. ��ͼ��ʾ�Ʊ�������þ�������н���������������ˡ�������������������ͭ���ˡ���������þ���ˣ����������õ��˹��˲�����˵����ȷ��
D. ��Һ���е����ʿ������Ȼ��ơ��Ȼ�þ���������������ƣ����Կ���Ϊ3�֣�˵������ѡD��

 �Ķ��쳵ϵ�д�
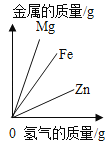
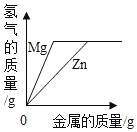
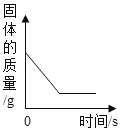
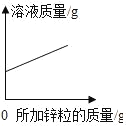
�Ķ��쳵ϵ�д�����Ŀ������ͼ������ȷ��ӳ��Ӧ�仯��ϵ���ǣ�������
|
|
|
|
Mg��Zn��Fe��ϡ���ᷴӦ | ������������������������������þ�ۡ�п�� | ��ͭƬ����һ��������������Һ�� | ��һ���������Ȼ�п��������Һ�м���п�� |
A. A B. B C. C D. D
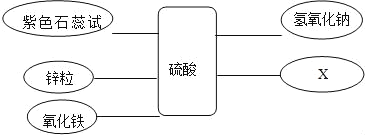
����Ŀ��MgSO4��Na2SO4��ԡ��ȱ����ܽ��������ͼ������˵����ȷ���� ��������
�¶�/�� | 20 | 30 | 40 | 50 | 60 | 70 | |
�ܽ�� S/g | MgSO4 | 33.7 | 38.9 | 44.5 | 50.6 | 54.6 | 55.8 |
Na2SO4 | 19.5 | 40.8 | 48.8 | 47.5 | 45.3 | 44.8 | |
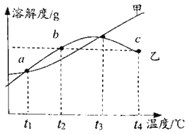
A. ��ΪNa2SO4
B. Ӧ����40��-50��֮��
C. �ҵı�����Һ�����µ��Ĺ����У�һֱ�о�������
D. b��c���ҵı�����Һ��������������ȣ��Ҵ���a��ı�����Һ������������