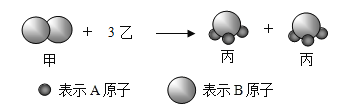
题目内容
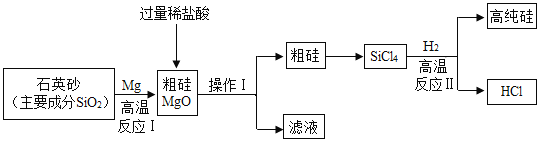
【题目】下图是初中化学常见物质间的转化关系(部分反应物、生成物及反应条件未标出),甲和G为组成元素相同的无色液体,F和H为组成元素相同的气体,I为磁铁矿的主要成分。试回答:
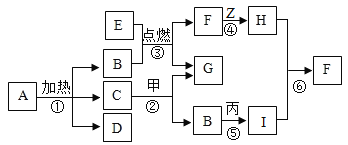
(1)反应②中C的作用是_____。
(2)写出相关反应的化学方程式:④_____;⑥_____。
(3)若有2.3g物质E在B中完全燃烧,生成4.4gF和2.7gG,则物质E中含有的元素是_____(填元素符号)。
【答案】催化作用 C+CO2 2CO 4CO+Fe3O4
2CO 4CO+Fe3O4 3Fe+4CO2 C、H、O
3Fe+4CO2 C、H、O
【解析】
I为磁铁矿的主要成分,则I是Fe3O4,甲和G为组成元素相同的无色液体,甲在C的催化作用下能够生成G和B,且A在加热的条件下能够生成B、C、D三种物质,所以A为KMnO4,C为MnO2,B为O2,D为K2MnO4,甲为H2O2,G为H2O,因为F和H为组成元素相同的气体,由反应④可知F为CO2,H为CO,乙为C,CO具有还原性,能够在高温条件下与Fe3O4反应生成Fe和CO2;
(1)反应②是二氧化锰催化过氧化氢分解的反应,该反应中,二氧化锰的作用是作催化剂;
(2)反应④是二氧化碳与碳在高温条件下生成一氧化碳的反应,该反应的化学方程式为C+CO2 2CO;反应⑥是一氧化碳在高温条件下与四氧化三铁的反应,产物为铁和二氧化碳,该反应的化学方程式为4CO+Fe3O4
2CO;反应⑥是一氧化碳在高温条件下与四氧化三铁的反应,产物为铁和二氧化碳,该反应的化学方程式为4CO+Fe3O4 3Fe+4CO2;
3Fe+4CO2;
(3)2.3g E在O2中完全燃烧,生成4.4g CO2和2.7g H2O,则产物中碳元素的质量=4.4g×![]() =1.2g,产物中氢元素的质量=2.7g×
=1.2g,产物中氢元素的质量=2.7g×![]() =0.3g,产物中氧元素的质量=4.4g×
=0.3g,产物中氧元素的质量=4.4g×![]() +2.7g×
+2.7g×![]() =6g,物质E中一定含有碳、氢元素,由于1.2g+0.3g=1.5g<2.3g,则物质E中还含有氧元素,因此物质E中含有的元素是C、H、O。
=6g,物质E中一定含有碳、氢元素,由于1.2g+0.3g=1.5g<2.3g,则物质E中还含有氧元素,因此物质E中含有的元素是C、H、O。