题目内容
【题目】用化学用语填空:
(1)铝元素_______________。(2)三个五氧化二磷分子______________________。
(3)两个氮原子___________。(4)三个硫酸根离子___________。
(5)保持氢气的化学性质的最小粒子是___________。
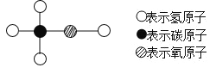
(6)甲烷中碳元素的化合价____________。
【答案】Al 3P2O5 2N 3SO42- H2 ![]()
【解析】
(1)铝的元素符号是Al。
(2)根据化学式的书写规则,五氧化二磷的化学式为P2O5,若要表示多个分子,直接在化学式的前面加上数字表示分子的个数,故3个五氧化二磷表示为3P2O5。
(3)原子直接用元素符号来表示,若要表示多个原子,在元素符号的前面加上数字,故2个氮原子表示为:2N。
(4)离子是在原子或原子团的右上角用数字加上正负号来表示,数字在前,正负号在后,数字是1时可以省略不写,若要表示多个离子,在离子符号的前面加上数字来表示,故3个硫酸根离子表示为:3SO42-。
(5)分子保持物质的化学性质,故氢气的化学性质是由氢气分子来保持,符号为H2。
(6)甲烷中氢元素的化合价为+1价,设碳元素的化合价为x,根据化合价的代数和为0,x+(+1)×4=0,x=-4,化合物中某元素的化合价标在该元素的正上方,故表示为:![]()

 名校课堂系列答案
名校课堂系列答案【题目】根据下图回答问题
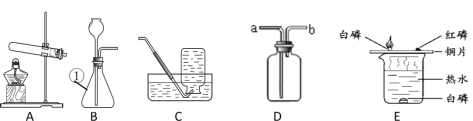
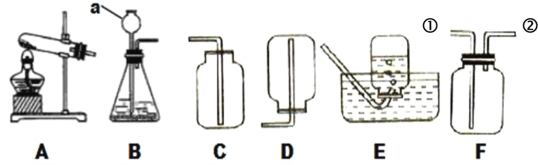
(1)仪器①的名称是__________。
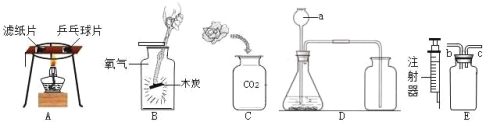
(2)B与C连接制取气体,反应的化学方程式为________。
(3)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷气的发生装置应选用____(填字母)装置;收集甲烷气可选用C装置,由此推断甲烷气具有的物理性质是_______。
(4)用图D的装置排水法收集氧气。瓶中装入水的量应为___(选:“少量”、“多量”或“满瓶”),进气口为____(选“a”或“b”)。
(5)E装置用来探究燃烧的条件,由铜片上白磷燃烧而红磷不燃烧得出的结论______。
(6)在实验室制取二氧化碳的研究中,进行了如下实验:
药品 | 甲 | 乙 | 丙 | 丁 |
大理石 | 2g,块状 | 2g,块状 | 2g,粉末状 | 2g,粉末状 |
盐酸(过量) | 20g,10%盐酸 | 20g,20%盐酸 | 20g,10%盐酸 | 20g,20%盐酸 |
Ⅰ、若要研究盐酸浓度大小对反应的影响,可选择实验甲与______对照(选填实验编号)。
Ⅱ、研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是_____(填字母序号)
①反应更为剧烈 ②最终剩余溶液的质量更小
③产生的二氧化碳的质量更大 ④粉末状大理石利用率更高
A.① B.①④ C.①③④ D.①②③④