题目内容
【题目】人类的生活和生产都离不开金属。

(1)下列生活用品中,主要利用金属导热性的是____________(填字母)。
(2)2019 年 8 月 30 日,新版第五套人民币发行,其中 5 角硬币的材质由原来的钢芯镀铜合金改为钢芯镀镍合金。选择铸造硬币的材料不需要考虑的因素是_________(填序号)。
A金属的导电性 B金属的耐腐蚀性 C金属的硬度 D金属价格与硬币面值的吻合度
(3)铁是应用最广泛的金属。①早在春秋战国时期,我国古代人民已经开始炼铁。写出磁铁矿与 CO反应的化学方程式___________。
②生活中铁制品容易生锈,用化学方程式表示除锈的原理是__________。
③目前世界上已有 50%以上的钢铁得到回收利用,其目的是__________(填序号)。
A节约金属资源 B合理开采矿物 C防止钢铁生锈
(4)在 AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,充分反应后过滤,得滤渣和滤液。若滤液呈无色,则滤渣中一定含有的物质是____________。
【答案】C A Fe3O4+ 4CO![]() 3Fe+4CO2 Fe2O3+6HCl=2FeCl3+3H2O A Ag 和 Cu
3Fe+4CO2 Fe2O3+6HCl=2FeCl3+3H2O A Ag 和 Cu
【解析】
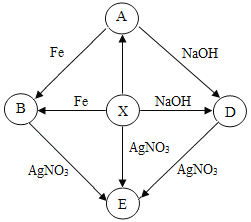
四氧化三铁和一氧化碳高温生成铁和二氧化碳,稀盐酸和氧化铁反应生成氯化铁和水,锌和硝酸银反应生成银和硝酸锌,锌和硝酸铜反应生成硝酸锌和铜。
(1)A、利用了金属铜的导电性,故A不正确;
B、黄金饰物利用了金特有的金属光泽,故B不正确;
C、铁能导热,可用铁锅做饭,故C正确;
D、铝制易拉罐是利用金属的延展性,故D不正确。故选C。
(2)5 角硬币的材质由原来的钢芯镀铜合金改为钢芯镀镍合金。选择铸造硬币的材料需要考虑金属的耐腐蚀性、金属的硬度、金属价格与硬币面值的吻合度,不需要考虑的因素是金属的导电性,故选A。
(3)①磁铁矿主要成分是四氧化三铁,与 CO高温反应生成铁和二氧化碳,反应的化学方程式为Fe3O4+ 4CO![]() 3Fe+4CO2。
3Fe+4CO2。
②铁锈的主要成分是氧化铁,稀盐酸和氧化铁反应生成氯化铁和水,反应的化学方程式表示为Fe2O3+6HCl=2FeCl3+3H2O。
③目前世界上已有 50%以上的钢铁得到回收利用,其目的是节约金属资源,故选A。
(4)金属活动性由强到弱的关系(Zn>Cu>Ag),锌先和硝酸银反应生成银和硝酸锌,反应完全,锌和硝酸铜反应生成硝酸锌和铜,充分反应后过滤,得滤渣和滤液,若滤液呈无色,说明锌和硝酸银、硝酸铜均反应完全,故滤渣中一定含有的物质是Ag 和 Cu。

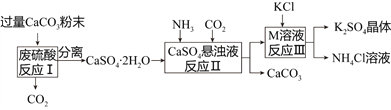
【题目】某化工厂用废硫酸制备K2SO4的流程如下:
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(1)生产上将CaCO3研成粉末的目的是________________________________________。
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是____________________(填写化学式);
(3)写出反应Ⅲ的化学方程式:___________________________________;你认为反应Ⅲ在常温下能实现的原因是__________________________________________________。
(4)洗涤反应Ⅲ所得晶体最好用下列_______(填序号),选择该试剂的原因是___________。
a.BaCl2溶液 b.饱和NH4Cl溶液 c.冷水 d.饱和K2SO4溶液