题目内容
【题目】某碳酸钠样品中含有一定量的氯化钠。为测定其纯度,取20 g样品于烧杯中,加入90g水搅拌形成不饱和溶液,往溶液中滴加氯化钙溶液100g至恰好反应,反应后过滤称得滤液的质量为200g。
(1)恰好反应产生的沉淀质量为______g。
(2)求样品中碳酸钠的质量分数?______
(3)求反应后滤液中溶质的质量分数?______
【答案】10g 53% 10.6
【解析】
(1)依据质量守恒定律可知,生成的CaCO3沉淀的质量为:20g+90g+100g-200g=10g;
(2)设样品中碳酸钠的质量为x,反应生成的氯化钠质量为y,
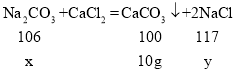
![]() x=10.6g,
x=10.6g,
![]() y=11.7g,
y=11.7g,
样品中碳酸钠的质量分数为:![]() ×100%=53%;
×100%=53%;
NaCl溶液质量分数为![]() ×100%=10.6%。
×100%=10.6%。

练习册系列答案
相关题目