题目内容
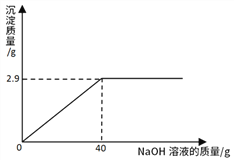
【题目】某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液。生成沉淀的质量与所用氢氧化钠溶液的质量关系下图所示。已知:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓。
(1)配制40g溶质质量分数为10%的NaOH溶液,需NaOH的质量=_______g。
(2)计算MgSO4溶液中溶质的质量分数为________________(列式计算)。
【答案】 4g 20%
【解析】(1)配制40g溶质质量分数为10%的NaOH溶液,需NaOH的质量为:40g×10%=4g;
(2)由反应的曲线可知,当加入40g氢氧化钠溶液时恰好完全反应;
设MgSO4溶液中溶质的质量为x,
MgSO4+2NaOH═Mg(OH)2↓+Na2SO4
120 80
x 40g×10%
![]()
x=6g,
MgSO4溶液中溶质的质量分数为:![]() ×100%=20%。
×100%=20%。

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
【题目】⑴请你判断下列化学式中的“2”分别表示下述哪种含义?
①表示离子的电荷数 ②表示微粒的数目 ③表示元素的化合价(填序号)2H______ ![]() ________________ Zn2+________
________________ Zn2+________
⑵判断下列物质的类别,并用相应的序号填空:
①单质 ②氧化物 ③酸 ④碱 ⑤盐
物质化学式 | P2O5 | Ca(OH)2 | H2CO3 |
物质类别 | _______ | _______ | _______ |