题目内容
【题目】一包干燥的红色粉末,由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成。下面是同学们的探究过程,请你参与并回答有关问题。
【提出问题】
猜想①:只有Cu 猜想②:只有Fe2O3
猜想③:只有Fe(OH)3 猜想④:是Fe(OH)3和Fe2O3的混合物
猜想⑤:是Cu、Fe2O3的混合物 猜想⑥是____的混合物
【查阅资料】
(1)2Fe(OH)3![]() Fe2O3+3H2O
Fe2O3+3H2O
(2)Cu溶解在Fecl3溶液中,得到FeCl2和CuCl2
[实验探究]
(3)甲同学进行下列实验,请你填写表中空白处。
实验操作步骤 | 实验现象 | 结论 |
①取用少量红色固体,放于试管中加热 | 固体没有明显变化,试管口附近内壁没有发现小液滴 | 红色固体不含________ |
②取少量红色粉末于试管中,滴加足量的稀盐酸 | 发现固体全部溶解,溶液变色 | 猜想_____可能成立,所可能涉及的化学反应方程式是___ |
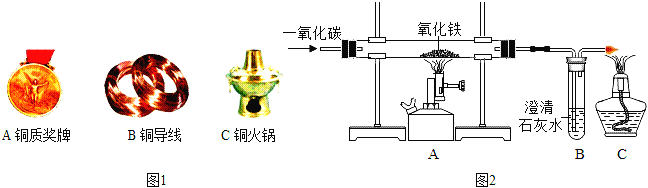
(4)在甲同学实验的基础上,乙同学为进一步确定红色粉末的组成,称取该粉末10.0g装入硬质玻璃管中,按右图装置进行实验。实验时发现澄清石灰水变浑浊,证明红色粉末中含有Fe2O3硬质玻璃管中发生反应的化学方程式是______反应完全后测得石灰水质量增加6.6g(假定CO足够多,石灰水足量,产生气体全部被吸收)则请计算出该红色粉末中各成分的质量____
【反思评价】丙同学指出:从环保角度,乙同学的实验装置有严重不足之处。请提出你的具体改进措施及原因:________________

【答案】 Cu,Fe(OH)3 Fe(OH)3 ②或⑤ Fe2O3+6HCL=2FeCL3+3H2O Cu+2FeCL3=2FeCL2+CuCL2 Fe2O3+3CO![]() 3CO2+2Fe Cu 2g Fe2O3 8g 应该将通过澄清石灰水的气体导到酒精灯火焰上燃烧掉或收集起来,以避免未反应的CO污染空气。
3CO2+2Fe Cu 2g Fe2O3 8g 应该将通过澄清石灰水的气体导到酒精灯火焰上燃烧掉或收集起来,以避免未反应的CO污染空气。
【解析】【提出问题】由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成,故猜想⑥是Cu,Fe(OH)3的混合物。【查阅资料】[实验探究](3)①取用少量红色固体,放于试管中加热,固体没有明显变化,试管口附近内壁没有发现小液滴,2Fe(OH)3△Fe2O3+3H2O,说明红色固体不含Fe(OH)3。②取少量红色粉末于试管中,滴加足量的稀盐酸,发现固体全部溶解,溶液变色,说明红色粉末中不能只有Cu,①中已经说明不含Fe(OH)3,而Fe2O3+6HCL=2FeCL3+3H2O,Cu+2FeCL3=2FeCL2+CuCL2 ,故猜想②或⑤可能成立,所可能涉及的化学反应方程式是Fe2O3+6HCL=2FeCL3+3H2O ,Cu+2FeCL3=2FeCL2+CuCL2 (4)硬质玻璃管中发生反应的化学方程式是:Fe2O3+3CO ![]() 2Fe+3CO2 ,石灰水能吸收二氧化碳,石灰水增加的质量是生成二氧化碳的质量,设该红色粉末中氧化铁的质量为x。
2Fe+3CO2 ,石灰水能吸收二氧化碳,石灰水增加的质量是生成二氧化碳的质量,设该红色粉末中氧化铁的质量为x。
Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
160 3×44
x 6.6g
![]() =
=![]() ,解得x=8g ,粉末中Cu的质量为:10.0g-8g=2g
,解得x=8g ,粉末中Cu的质量为:10.0g-8g=2g
【反思评价】应该将通过澄清石灰水的气体导到酒精灯火焰上燃烧掉或收集起来,以避免未反应的CO污染空气。