题目内容
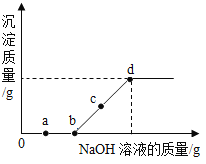
【题目】小红在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地发现有气泡产生,她认为氢氧化钠溶液已经变质。氢氧化钠溶液变质的原因是______(用化学方程式表示)。
小红对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:氢氧化钠部分变质,变质后的溶液中含有![]() 和
和![]()
猜想二:氢氧化钠全部变质,变质后的溶液中只含有![]()
(实验设计)为了验证猜想一,小红设计了如下方案:取少量变质后的氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变红色,说明溶液中含有氢氧化钠,氢氧化钠部分变质。小敏认为小红的实验方案不合理,理由是______。
(实验与结论)小敏另外设计实验方案验证猜想二,请你帮她完成下面的实验报告:
实验步骤 | 实验现象 | 结论 |
实验1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氧化钙溶液并振荡 | 有白色沉淀产生 | 猜想二正确 |
实验2:将实验1试管中的混合物过滤,______ | _______ |
实验1反应的化学方程式是______。
【答案】2NaOH+CO2![]() Na2CO3+H2O; 碳酸钠和氢氧化纳溶液都能使酚酞变红色; 向滤液中滴加无色酚酞溶液 无明显现象(或溶液不变红) Na2CO3+ CaCl2
Na2CO3+H2O; 碳酸钠和氢氧化纳溶液都能使酚酞变红色; 向滤液中滴加无色酚酞溶液 无明显现象(或溶液不变红) Na2CO3+ CaCl2![]() CaCO3↓+2NaCl
CaCO3↓+2NaCl
【解析】
氢氧化钠溶液变质,是因为和二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O。
[实验设计]
小敏认为小红的实验方案不合理理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
[实验与结论]
实验1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液并振荡,产生白色沉淀,是因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
实验2:将实验1试管中的混合物过滤,向滤液中滴加适量酚酞试液,酚酞试液不变红,说明溶液中不含氢氧化钠;
实验1反应的化学方程式是:Na2CO3+CaCl2═CaCO3↓+2NaCl。

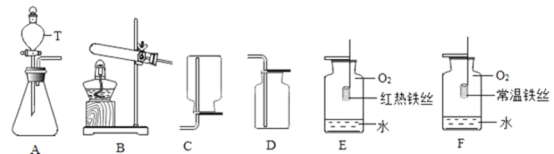
【题目】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:________________。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
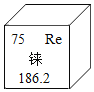
(提出猜想)除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。(完成实验)按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
实验标号 | 实验药品 | 分解温度(℃) |
① | KCI03 | 580 |
② | KCIO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO(质量比1:1) | 370 |
④ | KClO3、Fe203(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验________与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是________。
(反思)
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和__________不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证。
[提出猜想]质量相同的催化剂,颗粒越细,催化效果越好。
[设计实验]___________________________________________
[结论与反思]颗粒越细,与反应物接触面积越大,催化效果越好。