题目内容
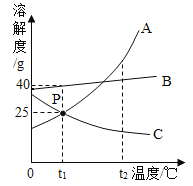
【题目】用质量分数为5%的氢氧化钠溶液中和10%的稀盐酸,反应过程中溶液的酸碱度变化如图25所示。
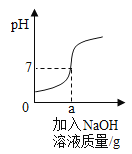
请回答:
(1)用质量分数为30%的浓盐酸配制10%的稀盐酸100g,需要水________________g (结果精确到0.1)。
(2)当a为160g时,消耗盐酸多少克?_______________
【答案】66.7g 73g
【解析】
设需要水的质量为x。
(100g-x)×30%=100g×10%
x≈66.7g
答:需要水的质量为66.7g。
(2)设氢氧化钠和盐酸恰好完全反应时,消耗HCl的质量为y。
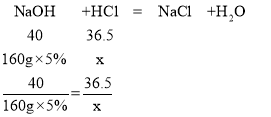
y=7.3g
消耗稀盐酸的质量为:7.3g÷10%=73g
答:当a为160g时所消耗稀盐酸73g。
故答案为:
(1)66.7;
(2)73g。

 备战中考寒假系列答案
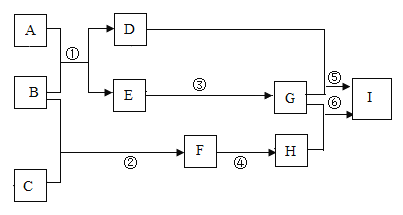
备战中考寒假系列答案【题目】把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是![]()
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为![]()
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1
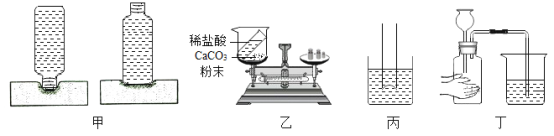
【题目】某化学兴趣小组的同学按图示装置验证氢氧化钠的化学性质。
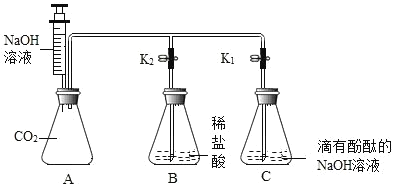
[实验步骤]
Ⅰ.关闭K1、K2,将注射器内的液体注入装置A中的锥形瓶内;
Ⅱ.打开K1,观察到装置C中部分红色溶液沿导管倒吸入装置A中,片刻后回流停止;
Ⅲ.打开K2,观察到装置B中溶液倒吸入装置A、C中,液面稳定后观察到装置A中溶液仍为红色,装置C中溶液变为无色。
同学们对相关问题分组展开如下探究:
探究环节 | 甲组的探究 | 乙组的探究 |
[提出问题] | 装置A中使酚酞变为红色的物质是什么? | 装置C中溶液为什么变成无色? |
[作出猜想] | 猜想一: Na2CO3; 猜想二: Na2CO3和NaOH | 猜想一:实验过程中酚酞变质了; 猜想二:溶液中的NaOH反应完了。 |
[实验验证] | ①小鹏取少量装置A中溶液于试管中,向其中滴加过量BaCl2溶液,若观察到_____,则证明猜想二成立; ②小丽认为用 | ①取少量装置C中溶液于试管中,向其中滴加NaOH溶液,溶液又变为红色,证明猜想一不成立; ②用pH试纸测定装置C 中溶液的酸|碱度,若pH_____, 则证明猜想二成立。 |
[反思交流]
(1)甲、乙两组同学的实验证明了NaOH能与稀盐酸、CO2发生反应,装置A中溶液里一定还存在NaCl;
(2)[实验步骤] II 中的现象_____(选填“能”或“不能”)证明NaOH与CO2发生了反应。
[拓展迁移]
综上所述,对于无明显现象的化学反应,要证明反应确实发生,可通过检验_____的方法实现。