题目内容
【题目】空气是一种重要的资源。
(1)工业上利用液化法分离出空气中的氧气和氮气,主要利用了氧气和氮气的__________(填“物理性质”或“化学性质”)。
(2)食品包装袋中常充氮气以防腐,所利用的氮气的性质是____________________。
(3)氧气和氮气的化学性质不同,请从微观角度说明理由:____________________。
(4)下图表示氧化汞生成汞和氧气的微观示意图:
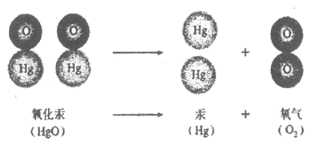
下列说法正确的是____________________。
A. 汞原子能保持汞的化学性质
B. 氧化汞分子由氧原子和汞原子构成
C. 此反应既是氧化反应,也是化合反应
D. 此过程中分子和原子的种类都发生了改变
E. 此化学变化过程,只是氧化汞分子分解成氧原子和汞原子的过程
【答案】物理性质 氮气的化学性质不活泼 氧气和氮气的分子不同 AB
【解析】
(1)工业上利用氧气和氮气的沸点不同,从液态空气中分离出氧气的过程属于物理变化;
(2)食品包装袋中常充氮气以防腐,所利用的氮气的性质是化学性质稳定;
(3)分子可以保持物质的化学性质,氮气的化学性质与氧气的化学性质不同是因为:氧气和氮气的分子不同;
(4)A、汞是由汞原子构成的,汞原子能保持汞的化学性质,故A正确;B、 氧化汞分子由氧原子和汞原子构成,故B正确;C、由微观示意图可知反应物是氧化汞,生成物是汞和氧气,该反应是由一种物质反应生成两种物质,属于分解反应,该反应不是物质与氧的反应,不属于氧化反应,故C错误;D、由图示可知:氧化汞分解过程中,氧化汞分子变成了汞原子和氧原子,氧原子与氧原子结合成氧分子,原子的种类没有发生改变,故D错误;E. 此化学变化过程,氧化汞分解时,不仅存在氧化汞分子变成了汞原子和氧原子的过程,还存在氧原子与氧原子结合成氧分子的过程,故E错误。故选AB。

【题目】取20g碳酸钠和碳酸氢钠的固体混合物,加热至不再产生气体2NaHCO3![]() Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
时间 | 0分钟 | 1分钟 | 2分钟 | 3分钟 |
仪器和浓硫酸的质量总和(g) | 150 | 150.9 | 151.8 | 151.8 |
(1)当完全反应后,生成水的质量为_____g。
(2)计算混合物中碳酸氢钠的质量分数________。(要求写出计算过程)
(3)将上述混合物完全分解后的固体溶解于186.2g 水中,待固体完全溶解后所得溶液中溶质的质量分数为_____。