��Ŀ����
����Ŀ��ij�о���ѧϰС������˲ⶨ���Na2CO3����Ʒ��ֻ��NaCl���ʣ���Na2CO3���������� ʵ�鷽������ش��������⣺
С���ϣ���ʯ�ҵ���Ҫ�ɷ����������ƺ������ƵĻ����
��1�����巨��
��ԭ��˼·������Na2CO3��ϡ���ᷴӦ����CO2��ͨ��������װ��ʵ��ǰ��������ó�CO2�������Ӷ�����̼���Ƶ�������������������ԭװ���ڿ�����Ӱ����
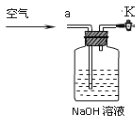
��ʵ�������С��ͬѧ��������˼·���������ͼʵ��װ�á�

��ʵ��װ������ʢ�ŵ��Լ�Ϊ ���������� ��
װ�ö��м�ʯ�ҵ������� ��������ĸ��
A.����Na2CO3��ϡ���ᷴӦ����CO2
B.��ֹ�������ж�����̼�������
C.���������̼
��ʵ��������μ�ϡ������ٶȹ��죬�ᵼ�²����Ʒ��̼���Ƶ��������� ����д��ƫ�ߡ�����ƫ�͡����䡱����
��С��ͬѧ��ΪС�Ƶķ����������⣬������ԭװ���ڿ�����Ӱ�죬��ʹ�����淶�����������ɵ�CO2��װ���в�����Ҳ����ɲ�ý�� ����д��ƫ�ߡ�����ƫ�͡����䡱����Ӧ�ý�װ�ü���˫����������������������������ͼװ�ã�ʵ�������ͨ��һ��ʱ�������Ŀ���� ������ͼ��NaOH��Һ�������� ��
��2����������
��ʵ��ԭ��������̼�������������ӽ�����ɳ�����ͨ���������������ó�̼���Ƶ�����������
��ʵ�鲽�衿����������ƽ��ȡ��Ʒ11.0g�����ձ��У���ˮʹ����ȫ�ܽ⣻
�ڼ��������CaCl2��Һ��ַ�Ӧ��֤��CaCl2������������Ʒ��Na2CO3��ȫ��Ӧ���ķ����ǣ����������ϲ���Һ�еμ� ��Һ�����û�а�ɫ�������ɣ�֤��CaCl2������
�۹��ˡ�ϴ�ӡ������������������Ϊ10.0g�����ڳ�������ճ����Һ������ϴ�Ӿͺ�ɣ������������������� ����д��ƫ�ߡ�����ƫ�͡����䡱����
��ͨ�������ṩ�����ݼ������Ʒ��̼���Ƶ�������������д��������̣����������0.1%����3�֣�ֻд����ѧ����ʽ��1�֣�
���𰸡���1����Ũ���ᣨ��ŨH2SO4�� ����ˮ�����������CO2�� B ��ƫ�� ��ƫ�ͣ� ��������CO2ȫ�����뵽��װ���У�ʹ����ȫ������������Һ���� �� ����ͨ��Ŀ����е�CO2
��2����CaCl2 �� ƫ�� ��96.4%
��������
�����������1��������̼������ϡ���ᷴӦ���ɵĶ�����̼�п��ܺ���ˮ���������ܻ�Ӱ��������������Ҫ�Զ�����̼���и������װ���е���Ũ����������к��ж�����̼����Ҫ�ü�ʯ�����տ����еĶ�����̼����ֹ��������������ж�����̼������Ӧ��
��ʵ���еμ�ϡ������ٶȹ��죬����������������������̼������ȫ������������Һ���գ����²����Ʒ��̼���Ƶ���������ƫ�ͣ�
�����ɵ�CO2��װ���в������ᵼ�¶�����̼���ܱ���������ȫ�����գ��ʻ���ɲ�ý��ƫ�ͣ�ʵ�������ͨ��һ��ʱ�������Ŀ���ǽ�������CO2ȫ�����뵽��װ���У�ʹ����ȫ������������Һ���գ�����ͼ��NaOH��Һ������������ͨ��Ŀ����е�CO2����ֹ�����еĶ�����̼���뵼�½��ƫ��
��2�����Ȼ��ƹ�����������Һ�е�̼������ȫ��Ӧ���ˣ�������Һ�м����μ��Ȼ��ƣ����Ƿ������������û�б�ʾ�Ȼ��ƹ�����̼������ȫ��Ӧ��
�۳�������ճ����Һ�����������Ȼ��ƣ�����ϴ�Ӿͺ�ɣ�������������������ƫ��
�����û�ѧ����ʽ������̼������̼��Ʒ�Ӧ�������ȼ��ɼ������Ʒ��̼���Ƶ�������
����Ʒ��̼���Ƶ�����Ϊx
Na2CO3+CaCl2![]() CaCO3��+2Na Cl
CaCO3��+2Na Cl
106 100
x 10.0g
![]() =
=![]()
x=10.6g
��̼���Ƶ�����������![]() ��100%��96.4%
��100%��96.4%
����




