جâؤ؟ؤعبف
،¾جâؤ؟،؟تµرéتزسذز»ئ؟±êا©²ذب±²¢ازئ؟¸اأ»سذحêب«أـ·âµؤخقة«بـز؛£¨بçدآح¼£©£¬»¯ر§ذ،×éµؤح¬ر§¾¹ر°ختہدت¦؛َض»ضھµہتاNaCl،¢NaOH،¢Na2CO3،¢NaHCO3ضذµؤز»ضضبـز؛£¬خھب·بدشئ؟ضذتا؛خضضبـضت²¢إذ¶دئنتا·ٌ±نضت£¬»¯ر§ذ،×éµؤح¬ر§½ّذذءثبçدآµؤج½¾؟»î¶¯£؛

،¾½ّذذ²آدë،؟
²آدëI£؛شبـز؛µؤبـضتتاNaCl£»
²آدëII£؛شبـز؛µؤبـضتتاNaOH£»
²آدëIII£؛شبـز؛µؤبـضتتاNa2CO3£»
²آدëIV£؛شبـز؛µؤبـضتتاNaHCO3،£
،¾²éشؤ×تءد،؟
³£خآدآ£¬سذ¹طخïضتµؤدà¹طذإد¢بçدآ±ي£؛
خïضت | NaCl | NaOH | Na2CO3 | NaHCO3 |
³£خآدآµؤبـ½â¶ب/g | 36 | 109 | 21.5 | 9.6 |
³£خآدآد،بـز؛µؤpH | 7 | 13 | 11 | 9 |
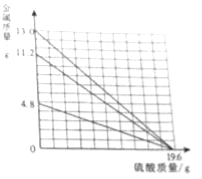
´سخïضتµؤدà¹طذإد¢؟ةضھ£¬شبـز؛µؤبـضتز»¶¨²»تاNaHCO3,زٍخھ_______،£
،¾½ّذذتµرé،؟
£¨1£©ب،ةظء؟رùئ·£¬²âµأبـز؛µؤpH´َسع7£¬شٍشبـز؛µؤبـضت؟د¶¨²»تا_______،£
£¨2£©ح¬ر§أاءيب،رùئ·سض½ّذذءثبçدآتµر飬تµرé¹³جبçدآ£؛
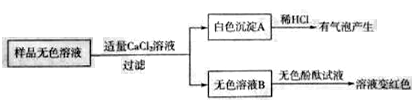
¢ظةْ³ة°×ة«³ءµيAµؤ»¯ر§·½³جت½__________________،£
¢عح¨¹تµرé؟ةزشإذ¶درùئ·خقة«بـز؛ضذ؛¬سذµؤبـضتسذ_______
،¾»ٌµأ½لآغ،؟
تµرéحê³ة؛َ£¬×îضصµأµ½µؤ½لآغ£؛شئ؟ضذµؤبـضتتا_____£¬اززر±نضت،£
،¾´ً°¸،؟،¾²éشؤ×تءد،؟£؛³£خآدآ£¬ج¼ثلاâؤئµؤبـ½â¶بتا9.6g£¬²»؟ةؤـµأبـضتضتء؟·ضتخھ10%µؤبـز؛،£،¾½ّذذتµرé،؟£¨1£©آب»¯ؤئ£¬£¨2£©¢ظCaCl2+Na2CO3=CaCl2،+2NaCl ،£¢عNa2CO3،¢NaOH£»،¾»ٌµأ½لآغ،؟NaOH
،¾½âخِ،؟،¾²éشؤ×تءد،؟£؛±¥؛حبـز؛بـضتµؤضتء؟·ضت=بـ½â¶ب،آ£¨بـ½â¶ب+100g£©،ء100% ،£³£خآدآ£¬ج¼ثلاâؤئµؤبـ½â¶بتا9.6g£¬²»؟ةؤـµأبـضتضتء؟·ضتخھ10%µؤبـز؛£¬شبـز؛µؤبـضتز»¶¨²»تاNaHCO3،£،¾½ّذذتµرé،؟£¨1£©آب»¯ؤئبـز؛³تضذذش£¬بـز؛µؤpHµبسع7£¬£¨2£©¢ظبـز؛ضذ¼سبëآب»¯¸ئةْ³ة°×ة«³ءµي£¬ثµأ÷بـز؛خھج¼ثلؤئبـز؛£¬زٍخھاâرُ»¯ؤئ²»سëآب»¯¸ئ·´س¦£»ج¼ثلؤئ؛حآب»¯¸ئ·´س¦ةْ³ةج¼ثل¸ئ³ءµي؛حآب»¯ؤئ£¬·½³جت½خھCaCl2+Na2CO3=CaCl2،+2NaCl ،£¢ع³¾،ج¼ثلؤئ؛َ£¬دٍبـز؛ضذ¼سبë·سجھتشز؛£¬·سجھتشز؛±ن؛ى£¬ثµأ÷سذ¼îذشخïضت£¬ض¤أ÷سذاâرُ»¯ؤئ£»سةةدتِتµرé؟ةض¤أ÷بـز؛ضذبـضتسذج¼ثلؤئ،¢اâرُ»¯ؤئ£¬زٍ´ث؟ةضھتازر¾±نضتµؤاâرُ»¯ؤئبـز؛،£

 أûذ£؟خجأدµءذ´ً°¸
أûذ£؟خجأدµءذ´ً°¸،¾جâؤ؟،؟تµرéج½¾؟جâ
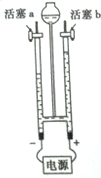
،¾تµرé»ط¹ث،؟18تہ¼حؤ©£¬س¢¹ْ؟ئر§¼زئصہûث¹جطہï؛ح؟¨خؤµدذي°ر،°ز×ب¼؟صئّ،±سë؟صئّ»ٍرُئّ»ى؛د؛َت¢شع¸ةشï،¢½à¾»µؤ²£ء§ئ؟ضذ£¬µ±سأµç»ً»¨µم»ًت±£¬·¢³ِصً¶ْµؤ±¬أùةù£¬از²£ء§ئ؟ؤعèµةد³ِدضءثز؛µخ،£ز»ؤêض®؛َ£¬ہحكخضط¸´ءثثûأاµؤتµر飬²¢×ِءثز»¸ِدà·´µؤتµرé£؛بأث®صôئّح¨¹ز»¸ùةص؛ىµؤا¹¹ـ£¬µأµ½ءث،°ز×ب¼؟صئّ،±،£صâہïµؤ،°ز×ب¼؟صئّ،±تاض¸________£¨جر§ت½£©£¬ح¨¹ةدتِتµرéµأµ½µؤ½لآغتا____________________،£
،¾تµرéضطدض،؟ؤ³»¯ر§ذثب¤ذ،×éµؤح¬ر§شع´´ذآµؤ»ù´،ةد£¬شعتµرéتزضذضط×ِةدتِء½¸ِتµر飬×ِ·¨بçدآ£؛
تµرé1£؛ث®µؤح¨µç·ض½âتµرé
بçسزح¼ثùت¾£¬´ٍ؟ھ»îبûb£¬سأب¼×إµؤؤ¾جُشع²£ء§¹ـ¼â×ى؟ع¼ىرé·´س¦²ْةْµؤئّجه£¬؟´µ½µؤدضدَتا________£¬ض¤أ÷¸أئّجهخھ_______،£
تµرé2: ،°ز×ب¼؟صئّ،±سëرُئّ»ى؛د؛َµؤµمب¼تµرé
تµرéتزدضسذ¹رُ»¯اâبـز؛،¢آبثل¼ط،¢¶رُ»¯أج،¢د،ءٍثل،¢ذ؟ء££¬زشدآتاتµرéتز³£سأ²؟·ضزائ÷£؛
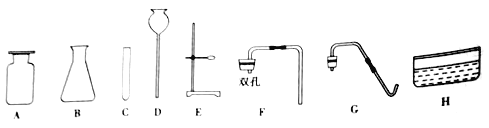
£¨l£©ض¸³ِح¼ضذزائ÷µؤأû³ئ:D______،£
£¨2£©ہûسأةدتِزائ÷؛حز©ئ·ضئب،ةظء؟رُئّ£¬ئن¼ٍز×·¢ةْ×°ضأس¦ر،شٌµؤزائ÷سذ_____£¨جîذٍ؛إ£©£¬·´س¦µؤ»¯ر§·½³جت½خھ______________،£
£¨3£©ہûسأةدتِزازئ؛حز©ئ·ضئب،½د¶àء؟µؤ،°ز×ب¼؟صئّ،±£¬از؟ةزشثوت±²¹³نز؛جه£¬ؤمر،شٌµؤزائ÷سذ_____£¨جîذٍ؛إ£©£¬ز©ئ·تا_____،£¸أذثب¤ذ،×éµؤح¬ر§°ر،°ز×ب¼؟صئّ،±سëرُئّ°´ز»¶¨±بہ»ى؛د؛َت¢شع¸ةشè،¢½à¾»µؤ²£ء§ئ؟ضذ£¬سأµç»ً»¨µم»ً£¬ث³ہûحê³ةةدتِتµرé،£
£¨4£©¸أذثب¤ذ،×éµؤح¬ر§¾ِ¶¨ہûسأضئµأµؤ،°ز×ب¼؟صئّ،±؛ح؟صئّ¼جذّ½ّذذج½¾؟£¬ثûأاب،7ض§تش¹ـ£¬زہ´خت¢ث®90%£¨جه»·ضت£©،¢80£¥،،شظسأإإث®¼¯ئّ·¨تص¼¯،°ز×ب¼؟صئّ،±£¬¶ّ؛َ·ض±ً°رتش¹ـ؟عزئ½ü¾ئ¾«µئµؤ»ًرو£¬تµرé½ل¹ûبçدآ±يثùت¾£؛
ذٍ؛إ | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
،°ز×ب¼؟صئّ،±جه»·ضت£¨%£© | 90 | 80 | 70 | 50 | 20 | 10 | 5 |
؟صئّجه»·ضت£¨%£© | 10 | 20 | 30 | 50 | 80 | 90 | 95 |
µمب¼دضدَ | °²¾² ب¼ةص | °²¾² ب¼ةص | بُµؤ ±¬أùةù | ا؟µؤ ±¬أùةù | ا؟µؤ ±¬أùةù | بُµؤ ±¬أùةù | ²»ب¼ةص ²»±¬أù |
·ضخِ±يضذذإد¢£¬حê³ةدآءذختجâ£؛
¢ظ شع»ى؛دئّجه±¬ص¨·¶خ§ؤع£¬،°ز×ب¼؟صئّ،± µؤجه»·ضتش¼خھ________£»
¢عؤم¶شب¼ةص»ٍب¼ةصجُ¼µؤذآبدت¶تا___________________،£
،¾جâؤ؟،؟ؤ³»¯ر§؟خجأخ§بئ،°ثل¼îضذ؛ح·´س¦،±£¬½«ر§ةْ·ض³ةبô¸ةذ،×é؟ھص¹ج½¾؟»î¶¯،£اëؤم؛حثûأاز»ئًحê³ةزشدآتµرéج½¾؟،£
،¾رفت¾تµرé،؟½«ز»¶¨ء؟د،رخثل¼سبëµ½ت¢اâرُ»¯¸ئبـز؛µؤذ،ةص±ضذ،£¸أ·´س¦µؤ»¯ر§·½³جت½تا_____________،£
،¾²éشؤ×تءد،؟CaC12 ¹ِز؛دشضذذش
،¾جل³ِختجâ،؟تµرéضذخ´¹غ²ىµ½أ÷دشدضدَ£¬²؟·ضح¬ر§²ْةْءثزةخت£؛·´س¦؛َبـز؛ضذبـضتµؤ³ة·ضتات²أ´£؟
،¾²آدëسë¼ظةè،؟صë¶شزةخت£¬¼××éح¬ر§²آدëبçدآ£؛
²آدëI£؛ض»سذCaC12 ²آدëII£؛سذ__________
²آدëIII£؛سذCaC12؛حCa(OH)2 ²آدëIV£؛سذCaCl2،¢HCl؛حCa(OH)2
زز×éح¬ر§¶شزشةد²آدëجل³ِضتزة£¬بدخھ²آدëIV²»؛دہي£¬ئنہيسةتا_________________،£
،¾تµرéج½¾؟،؟خھءثرéض¤ئنسà²آد룬¸÷ذ،×é½ّذذءثدآءذب¸ِ·½°¸µؤج½¾؟،£
تµرé·½°¸ | µخ¼س×دة«ت¯بïبـز؛ | ح¨بëCO2 | µخ¼سNa2CO3بـز؛ |
تµرé²ظ×÷ |
|
|
|
تµرéدضدَ | ____________ | __________ | ²ْةْ°×ة«³ءµي |
تµرé½لآغ | بـز؛ضذ؛¬سذCa(OH)2 | بـز؛ضذ؛¬سذCa(OH)2 | بـز؛ضذ؛¬سذCa(OH)2 |
،¾µأ³ِ½لآغ،؟ح¨¹ج½¾؟£¬ب«°àح¬ر§ز»ضآب·¶¨²آدëIIIتاصب·µؤ،£
،¾ئہ¼غ·´ث¼،؟£¨1£©±û×éح¬ر§بدخھµخ¼سNa2CO3بـز؛²ْةْ°×ة«³ءµي£¬²¢²»ؤـض¤أ÷بـز؛ضذز»¶¨؛¬سذCa(OH)2£¬اëؤم°ïضْثûأاثµأ÷شزٍ____________،£
£¨2£©شع·ضخِ·´س¦؛َثùµأبـز؛ضذبـضتµؤ³ة·ضت±£¬³ءث؟¼آاةْ³ةخïح⣮»¹ذèزھ؟¼آا_______،£