题目内容
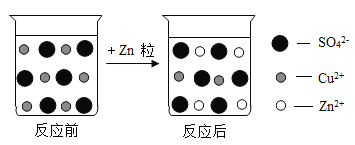
【题目】如图是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。
(1)锌与硫酸铜溶液发生反应过程中变化的微观粒子是 ______
(2)反应中过量的物质是_______(写化学式)。
(3) 该反应的化学方程式为________ 。
【答案】Zn 、Cu2+ CuSO4 Zn+CuSO4=ZnSO4 +Cu
【解析】
(1)由图知,锌与硫酸铜溶液发生反应过程中是Zn与Cu2+反应生成Zn2+和Cu的过程,所以变化的微观粒子是Zn 、Cu2+,故填:Zn 、Cu2+;
(2)由于反应后溶液中仍有铜离子存在,所以硫酸铜过量,故填:CuSO4;
(3)此反应的化学方程式为:Zn+CuSO4=ZnSO4 +Cu,故填:Zn+CuSO4=ZnSO4 +Cu。

【题目】某小组对“自制小火箭”的发射动力进行了如下探究。

(查阅资料)
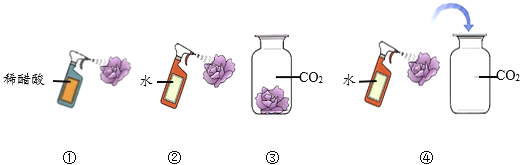
①火箭升空主要利用反冲原理:大量高温气体由火箭下方的喷气口向下喷出,使火箭获得向上的反作用力。当反作用力大于火箭受到的重力及空气阻力之和时,火箭飞离地面。
②醋酸化学性质与盐酸相似。
探究一:火箭发射的化学动力
同学们利用上图所示装置,选择不同的化学反应,在常温下进行火箭模拟发射实验,相关数据如下。
序号 | 实验组1 | 实验组2 | 实验组3 | |||||||||
H2O2溶液 | MnO2 质量 | 飞行距离 | 醋酸溶液 | Mg 质量 | 飞行距离 | 氧化钙质量 | 水 体积 | 飞行距离 | ||||
质量分数 | 体积 | 质量分数 | 体积 | |||||||||
1 | 7.5% | 100 mL | 1 g | 10.1 m | 15% | 100 mL | 1.2g | 10.6 m | 5 g | 100 mL | 0 | |
2 | 15% | 100 mL | 1 g | 12 m | 15% | 100 mL | 1.6g | 11.7 m | 10 g | 100 mL | 0 | |
3 | 30% | 100 mL | 1 g | 17 m | 15% | 100 mL | 2g | 12 .5m | 15 g | 100 mL | 0 | |
探究二:实验组3失败的原因
(猜想与假设)氧化钙固体已经变质,其成分可能是:
猜想1: CaCO3 猜想2:CaCO3和Ca(OH)2 猜想3:CaCO3、Ca(OH)2和CaO
(进行实验)
步骤Ⅰ.取少量固体样品于试管中,加入一定量的水,用手触摸试管外壁。
步骤Ⅱ.过滤。
步骤Ⅲ.取滤渣,滴加足量稀盐酸,观察现象。
步骤Ⅳ.试管外壁不发烫,酚酞溶液不变色。······
(解释与结论)
(1)探究一中,利用过氧化氢溶液作为火箭动力的化学反应方程式为_________________。
(2)探究一中,分析实验组1和实验组2的实验数据可知,火箭发射的化学动力与_______________因素有关。
(3)探究二中,步骤Ⅲ的实验目的是____________。
(4)探究二中,通过步骤Ⅳ得出滤液中不含氢氧化钙,则对应的操作及现象是____________。
(反思与评价)
(5)同学们讨论后一致认为:探究二中,根据步骤Ⅳ的现象,就可得出固体样品中一定没有______。
(6)实验室中的生石灰应__________保存。