题目内容
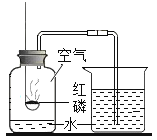
【题目】双球洗气管是一种多用途仪器,常用于去除杂质、气体干燥、气体吸收(能防止倒吸)等实验操作。下图是用水吸收下列某气体时情形,根据下列附表判断由左方进入的被吸收气体应是_____。
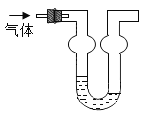
附:室温下四种气体的溶解度表
气体 | Cl2 | HCl | H2S | CO2 |
1体积水约能吸收气体体积数 | 2 | 500 | 2.6 | 1 |
【答案】HCl
【解析】
根据气体溶解度和造成的压强变化分析回答此题。
由题干信息可知,左侧液面升高,说明左侧压强减小,导致右侧大气压将水压入左侧,因此说明通入的气体极易溶于水,才会造成左侧压强减小,在四种气体中,只有氯化氢在水中极易溶解,造成压强减小,形成左侧水柱升高的现象,其余三种气体在水中溶解度较小,不足以引起足够的压强差,形成水柱。
故答案为:HCl。

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案【题目】分类、类比是学习化学常用的方法,掌握这些方法有助于学生学习化学知识。
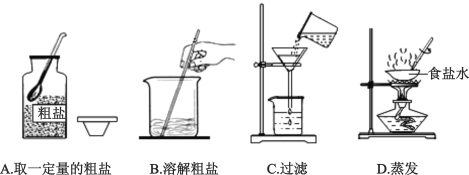
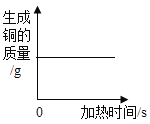
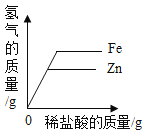
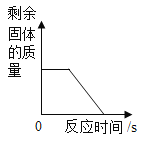
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究物质发生化学反应前后质量关系,探究物质的性质,探究物质的含量等。据此应将下列实验中的D与_______(填“A”或“B”或“C”)归为一类,依据是_____。
|
|
|
|
A | B | C | D |
(2)①电子数为 10 的粒子很多,其中包含电子数等于质子数的一些粒子。请将合适的化学符号填入空白HF、H2O、_____、CH4、Ne。
②查阅资料得知Mg、Mn、Fe、Cu四种金属活动性顺序是:“由强到弱”。若用实验验证这个结论,可以通过以下三个置换反应验证, 其中两个反应的化学方程式为:A.![]() 、B.
、B.![]() ,结合上述两个反应的化学方程式,请写出缺少的一个反应的化学方程式为_____。
,结合上述两个反应的化学方程式,请写出缺少的一个反应的化学方程式为_____。
【题目】铜片在空气中久置表面会变绿。某小组同学设计并进行实验,探究铜变绿的条件。
(查阅资料)(1)、铜绿的成分是碱式碳酸铜![]() ,碱式碳酸铜能够与盐酸反应。
,碱式碳酸铜能够与盐酸反应。
(2)、浓硫酸具有吸水性,可以作为一些气体的干燥剂。
(猜想与假设)常温下,铜片变绿可能与![]() 、
、![]() 、水蒸气有关。
、水蒸气有关。
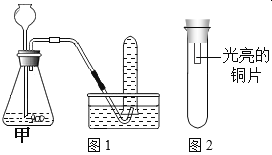
(进行实验)利用下图1装置分别制取并收集气体于试管中,制取气体原理及收集气体等操作见下表。将收集好的气体,用图2所示装置进行4个实验,通过控制与铜片接触的物质,进行实验并持续观察实验现象。
编号 | 主要实验操作 | 实验现象 |
1 | 甲中盛有过氧化氢溶液和二氧化锰,收集一试管气体 | 铜片始终无明显变化 |
2 | 甲中盛有大理石和稀盐酸,收集一试管气体 | 铜片始终无明显变化 |
3 | 甲处先用过氧化氢溶液和二氧化锰反应收集半试管气体,再换盛有大理石和稀盐酸的装置,继续收集至一试管气体 | 一段时间后铜片变绿 |
4 | 甲处先用过氧化氢溶液和二氧化锰反应收集半试管气体,再换盛有大理石和稀盐酸的装置,继续收集至一试管气体,并向气体中加入适量浓硫酸 | 铜片始终无明显变化 |
(解释与结论)
(1)实验1的目的是验证______。
(2)实验2制取气体反应的化学方程式为______。
(3)得出“铜片变绿一定与![]() 有关”的结论,依据的两个实验是______
有关”的结论,依据的两个实验是______![]() 填编号
填编号![]() 。
。
(4)实验4中,试管内的气体主要含有______。
(5)上述实验可推知,铜片变绿的条件是______。
(讨论与交流)
(6)同学们猜想碱式碳酸铜与盐酸反应有二氧化碳生成,证明此猜想所需试剂是______。