题目内容
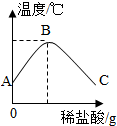 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:(1)由图知,稀盐酸与氢氧化钠溶液发生的反应是
(2)从A、到B过程中,烧杯中溶液的pH逐渐
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,物质发生化学变化时的能量变化,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)根据图象可以看出随着盐酸的加入温度在逐渐上升,据此进行分析解答.
(2)A到B的过程的反应实质是氢氧根离子逐渐减少,即氢氧化钠逐渐减少;B点对于温度是个转折点,对于反应进程也是个转折点,据此进行分析解答.
(2)A到B的过程的反应实质是氢氧根离子逐渐减少,即氢氧化钠逐渐减少;B点对于温度是个转折点,对于反应进程也是个转折点,据此进行分析解答.
解答:解;(1)由图象可以看出,随着稀盐酸的加入,温度在逐渐的升高,说明稀盐酸与氢氧化钠溶液发生的反应是放热反应,稀盐酸和氢氧化钠反应生成氯化钠和水,反应的化学方程式为 HCl+NaOH═NaCl+H20.
(2)由图是可知,从A到B过程中,氢氧化钠逐渐减少,碱性减弱,故pH值逐渐减小;在B点前后温度是两种情况,B点温度最高,B点表示酸碱恰好完全反应,反应后生成氯化钠和水,显中性,溶液中的pH=7.
故答案为:(1)放热;HCl+NaOH═NaCl+H20;
(2)变小/减小;酸碱恰好完全中和或酸碱恰好完全反应.
(2)由图是可知,从A到B过程中,氢氧化钠逐渐减少,碱性减弱,故pH值逐渐减小;在B点前后温度是两种情况,B点温度最高,B点表示酸碱恰好完全反应,反应后生成氯化钠和水,显中性,溶液中的pH=7.
故答案为:(1)放热;HCl+NaOH═NaCl+H20;
(2)变小/减小;酸碱恰好完全中和或酸碱恰好完全反应.
点评:本题难度不是很大,本题主要考查了结合图象考查了中和反应的应用,理解图象的含义、中和反应的实质是正确解答本题的关键.

练习册系列答案
相关题目
下列各组物质鉴别方法不正确的是( )
| A、用燃着的木条区别氧气、氢气和氮气 |
| B、用稀硫酸区分木炭粉、铁粉和氧化铜粉末 |
| C、用熟石灰区别化肥氯化铵、硝酸铵和硝酸钾 |
| D、用水区分无水硫酸铜、氯化钠和氢氧化钠固体 |
在一密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:则下列说法不正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 40 | 5 |
| 反应后质量/g | 待测 | 24 | 8 | 23 |
| A、该反应可能是置换反应 |
| B、参加反应的X 与Z的质量比为1:4 |
| C、反应后X的质量为0 |
| D、Y.Q的相对分子质量比一定为11:9 |
在AgNO3、Mg(NO3)2和Cu(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,滤液中存在的阳离子是( )
| A、Cu2+ |
| B、只有Fe3+ |
| C、Fe2+ |
| D、Mg2+、Fe2+ |
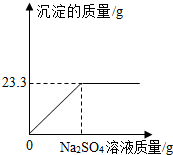 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl)
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl)