题目内容
现代信息技术的飞速发展对高纯度单质硅的需求急剧增加.请你用学过的知识回答下列问题:
(1)地壳中含有大量的硅元素,它的含量仅次于 元素;
(2)SiO2是沙子的主要成分,工业上制取硅的化学方程式为:SiO2+2C
Si+2R,R的化学式为 ,该反应的基本类型属于 ;
(3)硅能在氧气中燃烧生成SiO2,并放出大量的热,有科学家正研究将硅作为新能源.与化石能源相比,硅燃烧没有CO2放出,因而有助于解决的环境问题是 .
(1)地壳中含有大量的硅元素,它的含量仅次于
(2)SiO2是沙子的主要成分,工业上制取硅的化学方程式为:SiO2+2C
| ||
(3)硅能在氧气中燃烧生成SiO2,并放出大量的热,有科学家正研究将硅作为新能源.与化石能源相比,硅燃烧没有CO2放出,因而有助于解决的环境问题是
考点:地壳中元素的分布与含量,二氧化碳对环境的影响,反应类型的判定,质量守恒定律及其应用
专题:化学与环境保护,物质的微观构成与物质的宏观组成,化学用语和质量守恒定律
分析:(1)地壳元素含量最多的是氧,百分含量为百分之四十八点六,其次是硅和铝等八种元素.
(2)根据质量守恒定律可知,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.根据工业上制取粗硅的化学方程式和质量守恒定律就可计算出生成物各元素的原子个数与反应物各元素的原子个数之差,然后除以2,就是R的化学式中含有的元素的原子个数;根据化学方程式的特点确定反应类型;
(3)人类向大气中排入的二氧化碳等吸热性强的温室气体逐年增加,大气的温室效应也随之增强.硅燃烧没有CO2排放,因而有助于解决的环境问题是温室效应.
(2)根据质量守恒定律可知,在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.根据工业上制取粗硅的化学方程式和质量守恒定律就可计算出生成物各元素的原子个数与反应物各元素的原子个数之差,然后除以2,就是R的化学式中含有的元素的原子个数;根据化学方程式的特点确定反应类型;
(3)人类向大气中排入的二氧化碳等吸热性强的温室气体逐年增加,大气的温室效应也随之增强.硅燃烧没有CO2排放,因而有助于解决的环境问题是温室效应.
解答:解:(1)因为地壳元素含量最多的是氧,其次是硅.故答案为:氧;
(2)根据质量守恒定律和工业上制取粗硅的化学方程式(SiO2+2C
Si+2R)可知,R的化学式中应有的Si元素的原子个数为(1-1)÷2=0,O元素的原子个数为2÷2=1,C元素的原子个数为2÷2=1;则R的化学式为CO.故填CO;该反应是单质与化合物反应生成另外的单质和化合物的化学反应,属于置换反应;故填:置换反应.
(3)人类向大气中排入的二氧化碳等吸热性强的温室气体使大气的温室效应也随之增强,硅燃烧没有CO2排放,因而有助于解决的环境问题是温室效应.
故填:温室效应.
(2)根据质量守恒定律和工业上制取粗硅的化学方程式(SiO2+2C
| ||
(3)人类向大气中排入的二氧化碳等吸热性强的温室气体使大气的温室效应也随之增强,硅燃烧没有CO2排放,因而有助于解决的环境问题是温室效应.
故填:温室效应.
点评:本题主要考查学生运用化学方程式和化学式进行计算的能力,以及对地壳元素含量和温室效应的知识的认识.

练习册系列答案
相关题目
现取1.6g某有机物在足量的O2中完全燃烧,生成4.4gCO2和3.6gH2O.对该有机物组成有下列推断:( )
| A、一定含C、H 元素 |
| B、一定含有C、H、O元素 |
| C、一定不含C、O元素 |
| D、可能含有O元素 |
向一定量的硫酸溶液中,分别加入足量的水、金属锌、氢氧化钠溶液、氧化铜,下列图示正确的是( )
A、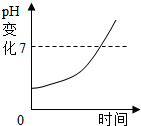 加足量水 |
B、 加足量锌 |
C、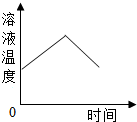 加足量NaOH溶液 加足量NaOH溶液 |
D、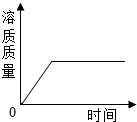 加足量氧化铜 加足量氧化铜 |
用分子的相关知识解释下列生活中的现象,其中错误的是( )
| A、“酒香不怕巷子深”,说明分子在不停运动 |
| B、分子由原子构成,说明分子比原子大 |
| C、20mL酒精和20mL水混合后体积小于40mL,说明分子间有间隙 |
| D、湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快 |
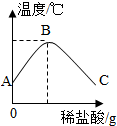 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示: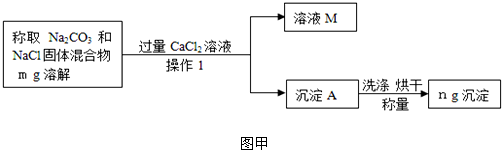
 人体中铁元素主要存在于血液中,是血红蛋白的成分,能帮助氧气的运输.如果体内缺铁会引起贫血.如图是某品牌补铁剂的药品标签.请回答:
人体中铁元素主要存在于血液中,是血红蛋白的成分,能帮助氧气的运输.如果体内缺铁会引起贫血.如图是某品牌补铁剂的药品标签.请回答: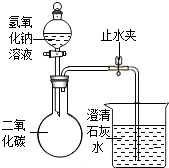 某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.