题目内容
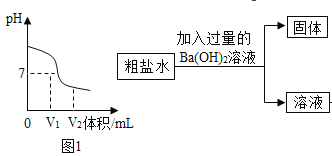
【题目】如图是氢氧化钠溶液和稀盐酸用滴加方式反应时,溶液 pH 随滴入溶液体积变化的曲线。
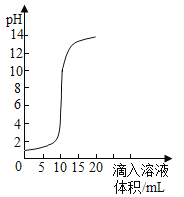
(1)根据曲线图判断,该反应是将__________(填“氢氧化钠溶液” 或“稀盐酸”)滴入另一种溶液中,实验过程中,随着反应的进行,溶液的温度逐渐升高,你认为溶液温度升高的原因是____________;
(2)写出氢氧化钠与稀盐酸反应的方程式___________, 从微观角度分析稀盐酸和 NaOH 溶液反应的实质是______;
(3)某同学在实验过程中,意外发现有气泡出现,你认为原因是_____________。
【答案】氢氧化钠溶液 氢氧化钠与稀盐酸反应放热; ![]()
![]() 氢氧化钠与空气中的二氧化碳反应生成了碳酸钠,碳酸钠与稀盐酸反应生成二氧化碳
氢氧化钠与空气中的二氧化碳反应生成了碳酸钠,碳酸钠与稀盐酸反应生成二氧化碳
【解析】
(1)根据曲线图可知,一开始pH<7,随着反应的进行,pH逐渐增大至大于7,故该反应是将氢氧化钠溶液滴入另一种溶液中;
实验过程中,随着反应的进行,溶液的温度逐渐升高,温度升高的原因是:氢氧化钠与稀盐酸反应放热;
(2)氢氧化钠与稀盐酸反应生成氯化钠和水,该反应的化学方程式为:![]() ;
;
从微观角度分析稀盐酸和 NaOH 溶液反应的实质是:![]() ;
;
(3)某同学在实验过程中,意外发现有气泡出现,可能是氢氧化钠与空气中的二氧化碳反应生成了碳酸钠,碳酸钠与稀盐酸反应生成二氧化碳。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案【题目】铁的锈蚀对社会生产造成损害,但也有有利的一面,如某些食品包装袋内常放入还原性铁粉作“双吸剂”以防止食品腐败。某同学发现了一包破损的还原性铁粉(含少量杂质,杂质既不溶于水也不溶于酸),他们取六份样品,分别加稀硫酸反应。测得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
取样品质量(g) | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 |
取稀硫酸质量(g) | 30.0 | 90.0 | 120.0 | 150.0 | 180.0 | 210.0 |
产生气体质量(g) | 0 | a | 0.3 | 0.5 | 0.6 | 0.6 |
(1)食品袋内放入“双吸剂”是为了吸收_____(填化学式),用铁粉而不用铁块作“双吸剂”的理由是_____。
(2)a的数值为_____。
(3)第4次实验,所得到溶液中溶质的化学式为_____。
(4)计算该样品中单质铁的质量分数_____(保留至0.1%)。