题目内容
【题目】化学与生活息息相关。请完成下面小题。
【1】二氧化碳在生活中应用广泛。
(1)干冰可用来冷藏食品,其原因是_________。
(2)二氧化碳可用于生产碳酸饮料,其中发生反应的化学方程式为_________。
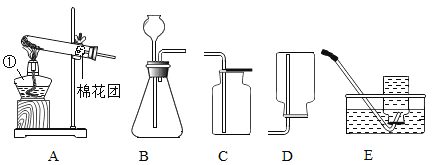
(3)实验室常用来检验二氧化碳的方法是_________(用化学方程式表示)。
【2】市售“自热米饭”的自加热原理:饭盒夹层中的水与生石灰(氧化钙)接触,发生化学反应:CaO + H2O = Ca(OH)2,放出大量热。该反应的基本反应类型为________。
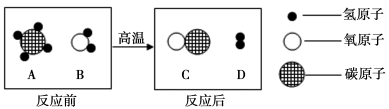
【3】汽车尾气系统中使用催化转化器,可降低有毒气体的排放,反应的微观示意图如下:
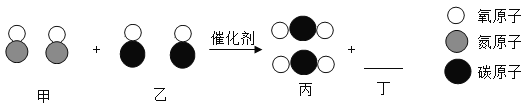
(1)请补全上图中相应微粒的图示______。
(2)当有0.56 g 乙被转化时,则同时被转化的甲的质量为________ g。
【答案】
【1】 干冰升华吸热 )![]()
![]()
【2】化合反应
【3】 ![]() 0.6
0.6
【解析】
1、根据二氧化碳的性质分析回答有关的问题,干冰易升华,二氧化碳能与水化合生成了碳酸,能与氢氧化钙反应生成了碳酸钙和水;
2、由多种物质生成一种物质的反应类型是化合反应;
3、观察化学反应的微观示意图,根据质量守恒定律,分析反应物、生成物,写出反应的化学方程式,根据方程式可以进行有关的计算。
【1】(1)干冰可用来冷藏食品,其原因是干冰升华吸热.
(2)二氧化碳可用于生产碳酸饮料,是由于二氧化碳能与水化合生成了碳酸,其中发生反应的化学方程式为:![]() ;
;
(3)由于能二氧化碳与氢氧化钙反应生成了碳酸钙沉淀和水,有明显的现象,实验室常用来检验二氧化碳,方程式是:![]() ;
;
【2】由反应:![]() ,可知反应物是两种,生成物是一种,属于化合反应;
,可知反应物是两种,生成物是一种,属于化合反应;
【3】由图示和质量守恒定律可知,在催化剂的作用下,一氧化碳和一氧化氮反应生成了氮气和二氧化碳,反应的化学方程式为:![]() ,
,
(1)由上述分析可知,丁应补充一个氮分子,图示为:![]() ;
;
(2)设被转化的甲的质量为X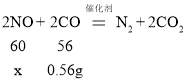
![]()
解得x=0.6g。

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
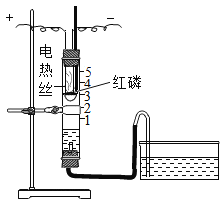
名校提分一卷通系列答案【题目】利用下图装置进行空气中氧气含量测定实验。
实验装置 | 实验操作 |
| I.向玻璃管和水槽内加适量的水,在燃烧匙里放足量红磷,塞紧塞子,上下移动水槽至两边水面相平于玻璃管的零刻度位置。 II.接通电源,待红磷燃烧,断开电源。 III.当温度恢复至室温,水不再进入玻璃管时,上下移动水槽至两边水面相平。 |
(1)实验中加入足量红磷的目的是_________。
(2)实验结束后,玻璃管内水面最终到达刻度线_______(填数字序号)处。
(3)实验操作I、III中,上下移动水槽至两边水面相平的目的是________。