题目内容
已知2.00%的硫酸铜溶液的密度为1.02g/mL.问:(1)该溶液的物质的量浓度是多少?
(2)欲配制500mL这种溶液需用CuSO4?5H2O晶体的质量是多少?
分析:(1)根据溶液的溶质质量分数与物质的量浓度间的关系,可借助数据假设的方法,由物质的质量分数推断出物质的量浓度;
(2)CuSO4?5H2O晶体溶于水所得硫酸铜溶液中,溶质硫酸铜即晶体中硫酸铜,溶剂水则为所加水与晶体中所含结晶水的和;根据这一特点,计算配制该溶液时所需要晶体的质量.
(2)CuSO4?5H2O晶体溶于水所得硫酸铜溶液中,溶质硫酸铜即晶体中硫酸铜,溶剂水则为所加水与晶体中所含结晶水的和;根据这一特点,计算配制该溶液时所需要晶体的质量.
解答:解:(1)假设该硫酸铜溶液体积1000mL即1L,则溶液中所含硫酸铜的物质的量=
=0.1275mol;
则该溶液的物质的量浓度=
=0.1275mol/L;
(2)500mL该溶液中所含量硫酸铜的质量=500mL×1.02g/mL×2.00%=10.2g,则需用CuSO4?5H2O晶体的质量=10.2g÷
×100%≈15.9g
答:(1)该溶液的物质的量浓度是0.1275mol/L;
(2)欲配制500mL这种溶液需用CuSO4?5H2O晶体的质量约为15.9g.
| 1000mL×1.02g/mL×2.00% |
| 160g/mol |
则该溶液的物质的量浓度=
| 0.1275mol |
| 1L |
(2)500mL该溶液中所含量硫酸铜的质量=500mL×1.02g/mL×2.00%=10.2g,则需用CuSO4?5H2O晶体的质量=10.2g÷
| 160 |
| 160+90 |
答:(1)该溶液的物质的量浓度是0.1275mol/L;
(2)欲配制500mL这种溶液需用CuSO4?5H2O晶体的质量约为15.9g.
点评:明确CuSO4?5H2O晶体溶于水所得硫酸铜溶液中溶质为硫酸铜,是解答此问题的基础.

练习册系列答案
相关题目
现有一种铜,氧化铁和炭的粉末状混合物,为测定该混合物中氧化铁的含量,某生取15g此样品置于烧杯中,分五次加入密度为1.10g/ml的硫酸溶液.有关数据记录如下表:
已知:在溶液中铜可与硫酸铁反应:Cu+Fe2(SO4)3=CuSO4+2FeSO4,第 5次加入硫酸溶液后剩余的固体中不含铜.
(1)所用硫酸溶液溶质的质量分数
(2)15.0g此样品中铜的质量.
(3)样品中氧化铁的质量分数.
| 加硫酸溶液的序号 | 加硫酸溶液的体积/ml | 剩余固体的质量/g |
| 1 | 30.0 | 10.52 |
| 2 | 30.0 | 6.04 |
| 3 | 30.0 | 2.2 |
| 4 | 30.0 | 0.6 |
| 5 | 30.0 | 0.6 |
(1)所用硫酸溶液溶质的质量分数
(2)15.0g此样品中铜的质量.
(3)样品中氧化铁的质量分数.
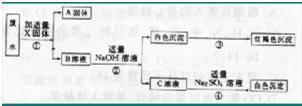
 (2012?南宁)据2012年4月15日中央电视台《每周质量报告》报道,一些不法厂商使用重金属铬超标的工业明胶代替食用明胶来生产药用胶囊.
(2012?南宁)据2012年4月15日中央电视台《每周质量报告》报道,一些不法厂商使用重金属铬超标的工业明胶代替食用明胶来生产药用胶囊.