题目内容
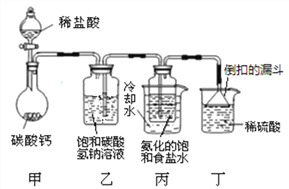
【题目】实验室常用块状大理石和稀盐酸反应制取CO2气体。某大理石中因含少量硫化物,使制得的CO2中混有H2S气体。某化学兴趣小组的同学欲用下图装置制取一瓶纯净、干燥的CO2,请回答下列问题:
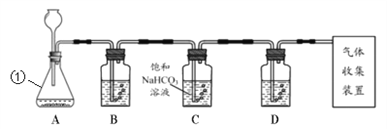
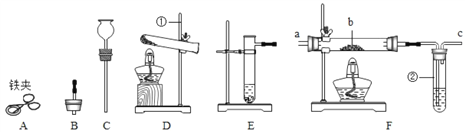
(1)仪器①的名称是____________;
(2)写出实验室制取二氧化碳的化学方程式_____________;找出装置A~D中的一处错误并加以改正:______________________,利用改正后的装置完成后面的实验;
(3)实验室制取的CO2中往往混有少量的HCl气体,其可能原因是___________________________;混有的HCl气体可用饱和NaHCO3溶液吸收。
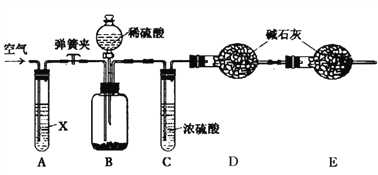
(4)小组同学查阅资料得知:H2S能与氢氧化钠溶液、硫酸铜溶液反应。欲除去CO2中混有H2S气体,B装置中所盛试剂应选用________(填“氢氧化钠”或“硫酸铜”)溶液,D装置的作用是_____________;
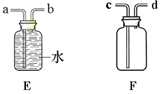
(5)用多功能瓶收集CO2的装置应选用________(填“E”或“F”),气体应从________(填“a”、“b”、“c”或“d”)端导管口通入。
【答案】 锥形瓶; CaCO3 + 2HCl = CaCl2 + H2O + CO2↑; 长颈漏斗未液封,长颈漏斗下端应伸入到液面下 盐酸浓度较高或盐酸有挥发性; 硫酸铜 除去水蒸气; F c
【解析】(1) (1)仪器①的名称是锥形瓶;(2)实验室常用石灰石或大理石与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;出装置A~D中的一处错误并加以改正:长颈漏斗未液封,长颈漏斗下端应伸入到液面下;(3)实验室制取的CO2中往往混有少量的HCl气体,其可能原因是盐酸浓度较高或盐酸有挥发性;混有的HCl气体可用饱和NaHCO3溶液吸收;(4)B装置中的碳酸氢钠溶液是用来除去二氧化碳中混有的氯化氢气体的,则装置甲中所盛试剂是用来除硫化氢气体的,且不与氯化氢反应,所以是硫酸铜溶液;B装置中的硫酸铜溶液除去了二氧化碳中混有的氯化氢气体,B装置中的碳酸氢钠溶液除去了二氧化碳中混有的氯化氢气体,则装置D是用浓硫酸来吸收二氧化碳中的水蒸气进行干燥;(5)二氧化碳能溶于水且密度比空气大,故用多功能瓶收集CO2二氧化碳的装置应选用F气体应从c端导管口通入。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:
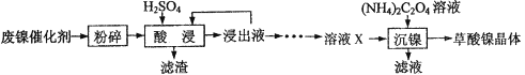
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
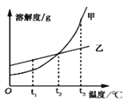
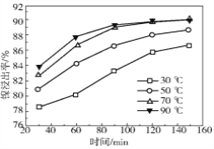
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。