题目内容
【题目】学习了元素的相关知识后相信同学们都有所收获,请根据所学的知识和提供的信息回答下列问题:

元素周期表的一部分
1 H | 2 He | ||||||
3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne |
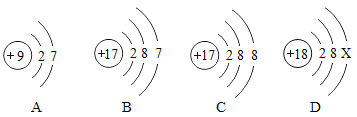
(1)图甲表示元素周期表中的一种元素,该元素属于 元素;(填“金属”或“非金属”),该元素原子中中子数为 ,图甲中表示的元素形成的离子结构示意图是 ;
(2)图乙表示的原子形成的离子符号为 ,该离子与 的核外电子排布相同。
【答案】(1)金属 12 (2)O2-Ne或氖原子
(2)O2-Ne或氖原子
【解析】
试题(1)图甲表示的元素属于金属元素;该元素原子中中子数为12;该元素形成的离子结构示意图是 ;
;
(2)图乙表示的原子是O,形成的离子符号为O2-,该离子与Ne或氖原子的核外电子排布相同。

练习册系列答案
相关题目