题目内容
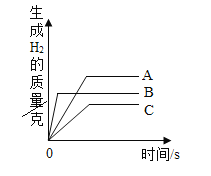
【题目】等质量的锌、铁与足量的稀硫酸反应,下列产生氢气的质量与反应时间的关系图,合理的是( )
A.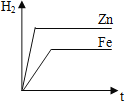 B.
B.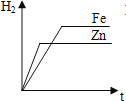 C.
C.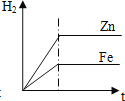 D.
D.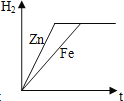
【答案】B
【解析】
由于稀硫酸过量,因此充分反应后放出氢气的质量大小由金属决定,根据化学方程式Fe+H2SO4=FeSO4+H2↑可以知道每56g铁生成2g氢气,根据化学方程式Zn+H2SO4=ZnSO4+H2↑可以知道每65g锌反应生成2g氢气,所以相等质量的铁和锌与足量硫酸反应铁生成氢气多,对于图象铁的终点纵坐标应该大于锌。根据金属活动性强弱关系锌>铁,可判断锌与稀硫酸反应快,铁与稀硫酸反应慢,即稀硫酸与锌的反应时间短、与铁的反应时间长。
A.等质量的铁和锌与足量硫酸反应,铁生成的氢气多,图像错误,不符合题意;
B.图像正确,符合题意;
C.等质量的铁和锌与足量硫酸反应,铁生成的氢气多,图像错误,不符合题意;
D.等质量的铁和锌与足量硫酸反应,铁生成的氢气多,图像错误,不符合题意。故选B。

练习册系列答案
相关题目