题目内容
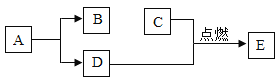
【题目】图 1 所示是等质量的甲、乙、丙、丁四种常见金属在容器中与盐酸的反应情况,卡通人周围的小黑 点表示反应中生成的气泡。
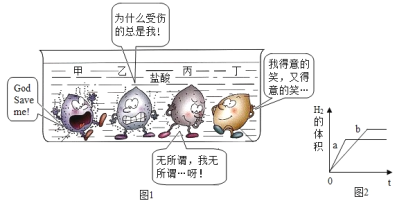
(1)甲、乙、丙、丁四种金属的 活动顺序中最弱的为_____。
(2)如果充分反应后,金属乙有 剩余,且表面已无气泡,则此时 溶液的溶质最多有_____种。
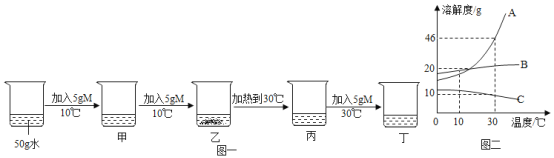
(3)若酸足量,图 2 中 a、b 分别表示其中两种金属的反应情况,则 a、b 可能是_____(填序号)
A a 为 Mg b 为 Al B a 为 Zn b 为 Cu C a 为 Mg b 为 Fe
【答案】丁 2 A
【解析】
(1)图中金属甲表面气泡最多,其次为金属乙,最少的为金属丙,金属丁表面无气泡,所以甲乙丙丁四种金属活动性由强到弱的顺序为:甲、乙、丙、丁,金属活动性最弱的为丁;
(2)根据图中的现象可知,甲、乙、丙会与酸反应,丁不会与酸反应,乙有剩余,乙会将丙从其盐溶液中置换出来,所以溶液中只有甲、乙的盐溶液,所以此时溶液中的溶质有2种;
(3)从图象可以看出,a比b活泼,b生成的氢气比a多,说明相同化合价时,b的相对原子质量比a小,
A、镁比铝活泼,24份质量的镁会生成2份质量的氢气,54份质量的铝会生成6份质量的氢气,相同质量的铝生成的氢气比镁多,符合题意,故A正确;
B、锌比铜活泼,但铜不与盐酸反应,不符合题意,故B不正确;
C、镁比铁活泼,24份质量的镁会生成2份质量的氢气,56份质量的铁生成2份质量的氢气,相同质量的镁生成的氢气比铁多,不符合题意,故C错误;
故选:A。

【题目】为了测定实验室中氯酸钾样品的纯度,某学习小组取2.5g该样品与0.5g二氧化锰混合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体的质量,重复以上操作,依次称得加热t1、t2、 t3、t4时间后剩余固体的质量,记录数据如下表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 2.48 | 2.34 | 2.04 | 2.04 |
请仔细分析实验数据,回答下列问题
(1)完全反应后产生氧气___________g
(2)该样品中氯酸钾的质量分数_________。