题目内容
【题目】某课外小组对氧化铜和铜的混合物成分进行探究。称取10g此样品,加入一定量的稀硫酸使之恰好完全反应,过滤后得到2g滤渣和溶质质量分数为10%的滤液。
(1)计算该样品中氧化铜的质量分数。
(2)根据化学方程式计算所得滤液中溶质的质量。
(3)计算所加入的稀硫酸的溶质质量分数?(计算结果精确到0.1%)
【答案】(1)80%;(2)16g;(3)6.4%
【解析】
(1)铜不与硫酸反应,而氧化铜可溶解于硫酸溶液,因此所得滤渣即铜的质量,该样品中氧化铜的质量分数![]() ,答:样品中氧化铜的质量分数是
,答:样品中氧化铜的质量分数是![]() 。
。
(2)、(3)设参加反应的![]() 的质量为x;生成
的质量为x;生成![]() 的质量为y。
的质量为y。
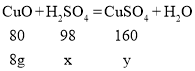
![]()
![]()
反应后所得硫酸铜溶液的质量![]() ,则消耗稀硫酸的质量
,则消耗稀硫酸的质量![]()
所加入的稀硫酸的溶质质量分数![]()
答:![]() 所得滤液中溶质的质量是16g;
所得滤液中溶质的质量是16g;
![]() 所加入的稀硫酸中溶质的质量分数为
所加入的稀硫酸中溶质的质量分数为![]() 。
。

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目