题目内容
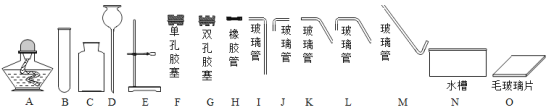
【题目】请结合下图回答问题。
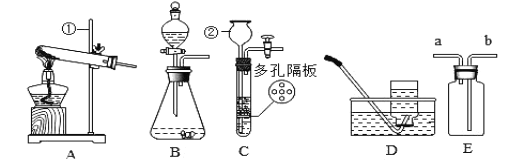
(1)仪器②的名称:________________。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置________________(选填序号)和装置D组合,反应的化学方程式为________________。若用B和D组合制取氧气,其反应的化学方程式为________________,若用E收集氧气,验满的方法是______________。
(3)实验室可用装置B或C制![]() ,C装置相对于B的优点有________________,用E装置收集
,C装置相对于B的优点有________________,用E装置收集![]() ,气体应从________________(选填“a”或“b”)端通入。
,气体应从________________(选填“a”或“b”)端通入。
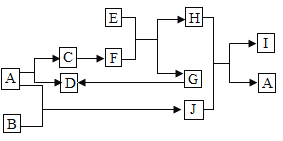
(4)利用纯净干燥的氢气与下列装置测定碱式碳酸镍晶体(![]() )组成,准确称3.77g样品进行如下实验(假设每个装置试剂足量,反应均完全)。试回答如下问题:
)组成,准确称3.77g样品进行如下实验(假设每个装置试剂足量,反应均完全)。试回答如下问题:
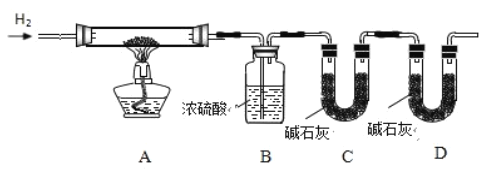
①装置C和D的作用分别是________________、________________。
②完全反应后装置A中得到1.77g金属,B增重1.62g、C增重0.44g。该样品中结晶水质量为_______________g,化学式为_______________。
③保持其他条件不变,仅将![]() 改为
改为![]() ,能否测定碱式碳酸镍的组成?________________(填“能”或“不能”)。
,能否测定碱式碳酸镍的组成?________________(填“能”或“不能”)。
【答案】长颈漏斗 A 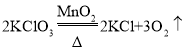
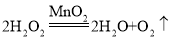 带火星的木条放在a导管口处,木条复燃,证明已满 能控制反应的发生与停止 a 吸收
带火星的木条放在a导管口处,木条复燃,证明已满 能控制反应的发生与停止 a 吸收![]() 防止空气中的
防止空气中的![]() 和
和![]() 从后面进入C中 0.72
从后面进入C中 0.72 ![]() 能
能
【解析】
(1)仪器②的名称长颈漏斗;
(2)用氯酸钾制氧气,反应物是固体,反应条件是加热,发生装置选用A;氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,反应的化学方程式为: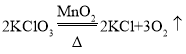 ;如果用双氧水和二氧化锰制氧气就不需要加热,若用B和D组合制取氧气所用药品是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为:
;如果用双氧水和二氧化锰制氧气就不需要加热,若用B和D组合制取氧气所用药品是过氧化氢溶液和二氧化锰,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为: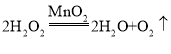 ;氧气的密度大于空气,若用E收集氧气,氧气应从b端通入,氧气具有助燃性,能使燃着的木条复燃,验满的方法是:把带火星的木条放在a处,木条复燃,证明氧气满了;
;氧气的密度大于空气,若用E收集氧气,氧气应从b端通入,氧气具有助燃性,能使燃着的木条复燃,验满的方法是:把带火星的木条放在a处,木条复燃,证明氧气满了;
(3)实验室可用装置B或C制H2,在装置C中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入。反应后关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。C装置相对于B的优点有:可以控制反应的发生和停止;用E装置收集H2,气体应从短管进入,因为氢气的密度比空气小;
(4)①装置C和D的作用分别是:吸收生成的二氧化碳;防止空气中的二氧化碳和水蒸气进入;
②碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O。NiO与氢气反应生成Ni和水。完全反应后装置A中得到 1.77g 金属,该金属为Ni。
设:生成1.77g的镍,需NiO的质量为a,同时生成水的质量为b。
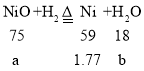
![]() a=2.25g
a=2.25g
![]() b=0.54g;
b=0.54g;
浓硫酸具有吸水性,B增重 1.62g是反应生成水的质量,碱式碳酸镍晶体受热会完全分解生成水的质量=1.62g-0.54g=1.08g,碱石灰能吸收二氧化碳,C增重 0.44g是反应生成的二氧化碳质量。
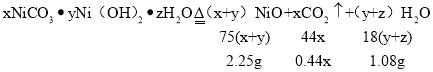
![]() y=2x
y=2x
![]() z=4x
z=4x
计算xNiCO3yNi(OH)2zH2O中x:y:z=1:2:4,所以化学式为;
=3.77g﹣1.77g﹣0.44g=1.56g;化学式为:NiCO3Ni(OH)24H2O;该样品中结晶水质量=![]() ;
;
③保持其他条件不变,仅将 H2改为 N2,可通过测定反应后A、B、C的质量,通过![]() 分解的化学方程式可计算出x、y、z的比值从而确定碱式碳酸镍的组成;
分解的化学方程式可计算出x、y、z的比值从而确定碱式碳酸镍的组成;

 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案