题目内容
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答:

(1)OA段无沉淀产生,请写出反应的化学方程式 ;
(2)加入镁粉的质量为 g;
(3)求产生氢气的质量是多少g?(写出计算过程,保留小数点后一位).

(1)OA段无沉淀产生,请写出反应的化学方程式 ;
(2)加入镁粉的质量为 g;
(3)求产生氢气的质量是多少g?(写出计算过程,保留小数点后一位).
(1)H2SO4+2NaOH=Na2SO4+2H2O; (2)2.4 (3)0.2g
试题分析:(1)开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水,反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O;故填:H2SO4+2NaOH=Na2SO4+2H2O;
(2)生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量,由图可知生成氢氧化镁的质量为5.8g,所以加入镁粉的质量=
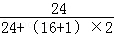 ×100%×5.8g=2.4g;故填:2.4;
×100%×5.8g=2.4g;故填:2.4;(3)设氢气的质量为x.
H2SO4+Mg=MgSO4+H2↑
24 2
2.4g x
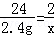
x=0.2g
答:产生氢气的质量是0.2g.
点评:本题主要考查学生利用化学方程式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
 2Fe+3CO2。
2Fe+3CO2。
 .试求:
.试求:
 K2S + 3CO2↑+ N2↑。若该反应消耗64 g硫,计算生成CO2的质量。
K2S + 3CO2↑+ N2↑。若该反应消耗64 g硫,计算生成CO2的质量。