��Ŀ����
����Ŀ��������������ֽ����Ⱦ��ϡ�ͼ���ҽҩƷ�ȵ���Ҫԭ�ϡ�ij�����ƴ�Ʒ�к����������Ȼ��ơ��Ȼ�þ��ʵ���ҽ����ᴿ���������£�
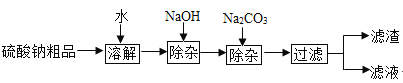
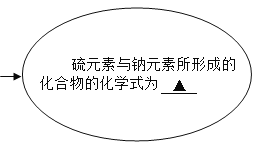
��1��������������Ҫ�ɷֵĻ�ѧʽΪ_____________
��2��NaOH �� Na2CO3 ������ӹ����ˣ��ɼ�������____��Һ��ȥ��
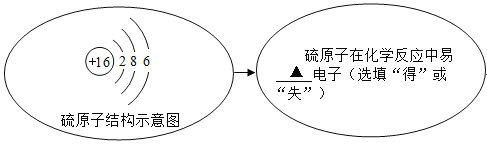
��3������������������Ҫ������������Ϊ�˻�ô����������ƣ�Ӧ������_____��ѡ����ĸ����
A ��ȫ����ʱֹͣ����
B �д�����������ʱֹͣ���ȣ�������������
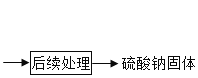
��4����֪�����Ƶ��ܽ�����¶ȱ仯��������ͼ��ʾ��40��ʱ�������Ƶı�����Һ��������������Ϊ__________�������ȷ��0.1%�������ñ�����Һת��Ϊ���¶��²�������Һ�ķ�����_________ ��_______
���𰸡�Mg(OH)2��CaCO3 ϡ���� B 33.3% �����ܼ� ���������º����ٻָ���ԭ���¶�
��������
��1�������ƴ�Ʒ�к����������Ȼ��ơ��Ȼ�þ����������������Ϊ�˳�ȥ�Ȼ�þ�������ķ�Ӧ����ʽΪ![]() ������̼������Ϊ�˳�ȥ�Ȼ��ƣ������ķ�Ӧ����ʽΪ
������̼������Ϊ�˳�ȥ�Ȼ��ƣ������ķ�Ӧ����ʽΪ![]() ���������е�������Ҫ�ɷ���Mg(OH)2��CaCO3��
���������е�������Ҫ�ɷ���Mg(OH)2��CaCO3��
��2��NaOH ��H2SO4��Ӧ���������ƺ�ˮ�� Na2CO3��H2SO4��Ӧ���������ơ�������̼��ˮ�����ɳ����ֲ����������ʣ����Կɼ�������ϡ������Һ��
��3��������������ʱ������Ҫ��ȫ���ɣ��д�����������ʱ����ֹͣ���ȣ��������Ƚ������ɣ���ѡB��
��4����ͼ���֪��40��ʱ�������Ƶ��ܽ��Ϊ50g������ɱ�����Һ�����ʵ���������Ϊ![]() ������40��ʱ�����Ƶ��ܽ�ȴﵽ���ֵ����ʱ�����������¶Ȼ��ǽ����¶ȣ�����ʹ�����Ƶ��ܽ���½�����ɱ�����Һ�о������������Խ��ñ�����Һת��Ϊ���¶��²�������Һ�ķ��������������ܼ���Ҳ�������������º��������ľ�����ٻָ���ԭ���¶ȡ�
������40��ʱ�����Ƶ��ܽ�ȴﵽ���ֵ����ʱ�����������¶Ȼ��ǽ����¶ȣ�����ʹ�����Ƶ��ܽ���½�����ɱ�����Һ�о������������Խ��ñ�����Һת��Ϊ���¶��²�������Һ�ķ��������������ܼ���Ҳ�������������º��������ľ�����ٻָ���ԭ���¶ȡ�

 ȫ��������ϵ�д�
ȫ��������ϵ�д� һ��һ����ʱ���ϵ�д�
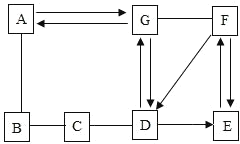
һ��һ����ʱ���ϵ�д�����Ŀ����ͼ��ʵ�����Ʊ�����IJ���װ�á�
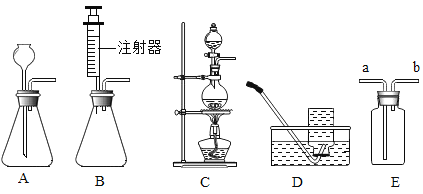
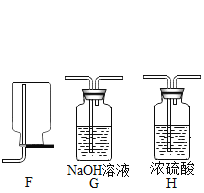
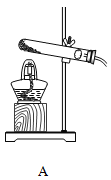
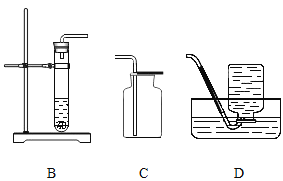
��1����ͼװ�ÿ�����ȡ��ͬ���壬������±��ո�
��Ӧ��ͷ�Ӧ���� | ��ȡ������ | ����װ�ã�����ĸ�� | �ռ�װ�ã�����ĸ�� |
��H2O2��Һ��MnO2���壬���� | _____ | A��B | _____��E |
���������ƣ�Na2SO3�������Ũ���ᣬ���� | SO2 | _____ | E |
�ۼ��ᣨHCOOH����Ũ���ᣬ���� | CO | _____ | D |
��2����Aװ����ȡO2ʱ����Ӧ�Ļ�ѧ����ʽΪ_____����Ҫ�õ������O2����ѡ��װ�õ�����˳��Ϊ��A��_____��E������ĸ��ţ���
��3����Eװ���ռ�SO2ʱ������Ӧ�ɣ��a����b����_____�˽��롣