题目内容
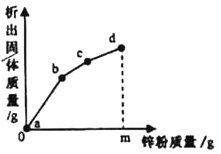
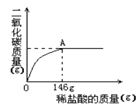
【题目】现取25 g石灰石样品,加入溶质质量分数为l 0%的稀盐酸,生成的二氧化碳与加入稀盐酸的质量关系如图所示(石灰石的主要成分是碳酸钙,杂质不溶于水也不与酸发生反应)。
求:(1)当反应进行到A点时,消耗的稀盐酸中溶质的质量(过程和结果);
(2)石灰石样品中碳酸钙的质量分数。
【答案】14.6g 80%
【解析】(1)当反应进行到A点时,恰好完全反应,消耗的稀盐酸中溶质的质量∶146g×l0%=14.6g。(2)石灰石样品中碳酸钙的质量分数∶
解∶设石灰石样品中碳酸钙的质量分数为x
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 73
25g×x![]() 14.6g
14.6g
![]() =
=![]() ,x=80%。
,x=80%。
答∶(1)当反应进行到A点时,消耗的稀盐酸中溶质的质量是14.6g。
(2)石灰石样品中碳酸钙的质量分数是80%。
点睛∶根据化学方程式进行计算,前提是正确书写化学方程式。有关含杂物质的计算应先把含杂物质转化为纯净物,再代入化学方程式进行计算。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】水是生命之源,人类的生产、生活离不开水。
(1)硬水给生活和生产带来很多麻烦,生活中可用___________来区分硬水和软水,常用______的方法来降低水的硬度。
(2)在利用太阳能使水分解获取清洁氢能的过程中,太阳能转化为_______能。此过程发生反应的化学方程式为__________。
(3)水变成水蒸气的过程中,下列变化正确的是_________(填序号)
A.水分子质量减小 B.水分子变大 C.水分子间隔变大 D.水分子体积增大
(4)根据下表回答相关问题。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度(g/100g水) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
①上表中两种物质的溶解度相等的温度范围是在____________℃
②20℃时,硝酸钾的溶解度是31.6g,其含义是______________。该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是______。要进一步提高该溶液的溶质质量分数,可进行的操作是_________。
【题目】化学就在我们身边,人类的衣、食、住、行都离不开化学。
⑴星期天小明和班里的几个同学到郊外去野炊。
①早上出门时,小明选择了一件腈纶衬衣,它是由________(填“天然”或“合成”)材料制成的。
②上午游玩时,闻到了远处扑鼻的花香,说明了__________________。
③中午他们准备的食物和饮料有:咸味烤饼、牛奶、烤肉串、米饭、矿泉水。从均衡膳食角度,还需要补充的食物是___________。
④下午离开时,他们用泥沙覆盖火堆,使火熄灭。这种灭火方法的原理是__________。
⑵为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题。
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
①物质C是由________构成(填“分子”、“原子”或“离子”)。
②以上4种物质中属于氧化物的是__________(填字母序号)。
③该反应中C、D两种物质的质量比为_________。
④D物质在空气中燃烧的化学方程式为:____________。
【题目】把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是![]()
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为![]()
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1