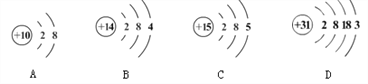
题目内容
【题目】写出下列化学方程式。
(1)电解水___________________
(2)二氧化碳通过炽热的焦炭层___________________
(3)加热氯酸钾与二氧化锰的混合物___________________
(4)一氧化碳还原氧化铁___________________
【答案】 2H2O![]() 2H2↑+O2↑ CO2+C
2H2↑+O2↑ CO2+C![]() 2CO 2KClO3
2CO 2KClO3 ![]() 2KCl+3O2↑ 3CO+Fe2O3
2KCl+3O2↑ 3CO+Fe2O3 ![]() 2Fe+3CO2
2Fe+3CO2
【解析】本题考查学生根据反应原理书写化学方程式的能力,化学方程式书写时注意化学式正确书写,配平,不要遗忘写条件、标符号等。
(1)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
(2)二氧化碳通过炽热的焦炭层,生成一氧化碳,反应的化学方程式为:CO2+C![]() 2CO;
2CO;
(3)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3 ![]() 2KCl+3O2↑;
2KCl+3O2↑;
(4)一氧化碳还原氧化铁生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3 ![]() 2Fe+3CO2。
2Fe+3CO2。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案【题目】工业上生产电石(CaC2)制备重要工业原料乙炔(CxHy)流程如下:
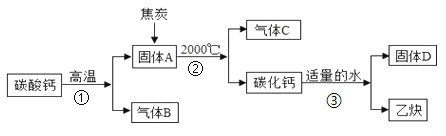
请回答下列问题:
(1)写出碳酸钙高温分解①的化学方程式____________________;B、C组成的元素相同,C有毒,则反应②的化学方程式____________________;根据反应③可推断固体D中一定含有的元素是____________________。
(2)已知:浓硫酸具有强吸水性。一个乙炔分子由4个原子构成。为了测定乙炔的组成,将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过下图的__________(选填“甲”或“乙”)装置,再缓缓通过一段时间的N2,缓缓通过一段时间的N2的目的是__________。
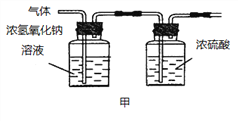
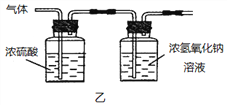
记录实验数据如下:
装置 | 反应前质量 | 反应后质量 |
浓硫酸 | 125.3g | 127.1g |
浓氢氧化钠溶液 | 78.2g | 87.0g |
根据实验数据推断乙炔的化学式(写出推断过程):__________