题目内容
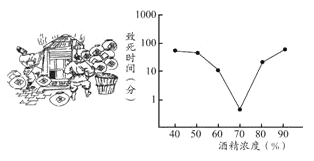
【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.

提出问题:久置固体的成分是什么?
查阅资料:铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
作出猜想:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
实验探究:
甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
取少量固体放于试管中,滴加足量的_____. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有_____, 一定不含Fe2O3. |
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_____.并设计如下实验方案继续验证.
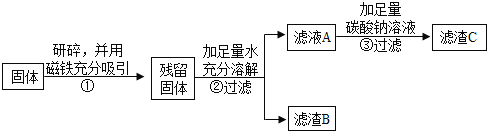
(1)②中固体溶解时放出大量热,由此可以判断固体中一定含有_____.
(2)③中反应的化学方程式是_____.
乙同学对滤渣B又进行探究.
实验操作 | 实验现象 | 实验结论 |
_____ | _____ | 固体中一定含有CaCO3 和Fe2O3. |
丙同学认为乙同学的方案中仍有一种物质不能确定.丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
综合上述实验及所给数据,久置固体的成分是_____.
【答案】甲同学的方案:稀盐酸 Fe
乙同学理由:氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色。
(1)CaO
(2)Na2CO3+ Ca(OH)2= CaCO3↓+ 2NaOH
对滤渣B的探究
实验操作 | 实验现象 | 实验结论 |
①取滤渣B于试管中,加入适量稀盐酸。 | ①固体减少,有气泡冒出,溶液变为黄色。 |
【实验结论】Fe、Fe2O3、CaO、Ca(OH)2、CaCO3
【解析】
[实验探究]
取少量固体放于试管中,滴加足量的稀盐酸,有大量无色气体产生,得到浅绿色溶液,固体中一定含有铁,不一定不含Fe2O3,因为氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色。故答案为:稀盐酸;Fe;氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色。
(1)氧化钙与水反应放热,故②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO。
(2)氧化钙与水反应生成氢氧化钙,滤液A中一定有氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,③中反应的方程式为:Na2CO3+ Ca(OH)2 = CaCO3↓+ 2NaOH。
对滤渣B的探究:
取滤渣B于试管中,加入适量稀盐酸,固体减少,有气泡冒出,溶液变为黄色;
将生成的气体通入澄清石灰水,澄清石灰水变浑浊;固体中一定含有CaCO3和Fe2O3。
[实验结论]
综合上述实验及所给数据,久置固体的成分是:Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。

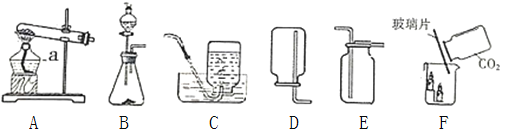
【题目】铝粉和氧化铁粉末反应(铝热反应).实验装置如图:
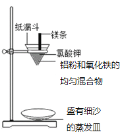
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式___.该反应中单质铝与一氧化碳有相似的___(填“氧化”或“还原”)性.在这一实验过程中没有涉及的基本反应类型是___.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
(提出问题)任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
(实验方案)
实验组别 | 实验操作 | 实验现象 | 结论 |
实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成___色固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈___色. | ___ |
实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
(实验总结)金属与金属氧化物在高温条件下有些能反应,有些不能反应.
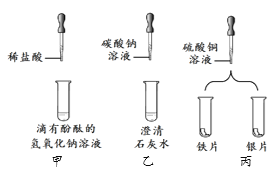
【题目】在宏观、微观和符号之间建立联系是化学学科的特点.
(1)在氧气、汞和氯化钠3种物质中,由离子构成的是_____.
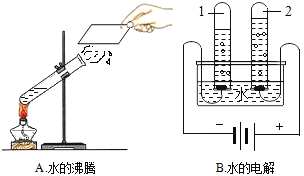
(2)如图所示的2个实验,从微观粒子的角度分析,两种变化的本质区别是_____,通过B实验证明水是由_____组成的.
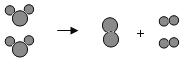
(3)A、B、C、D表示4种物质,其微观示意图见下表.
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
A和B在一定条件下反应可生成C和D.下列说法正确的是_____(填序号).
①4种物质均由分子构成 ②4种物质中D属于单质 ③该反应属于置换反应 ④反应前后各元素化合价均未改变 ⑤生成C、D两种物质的质量比为22:7.
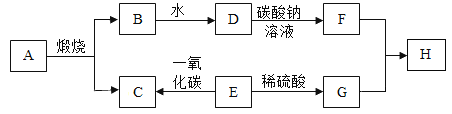
【题目】甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
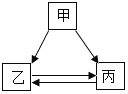
选项 | 甲 | 乙 | 丙 |
A | H2O2 | O2 | H2O |
B | KOH | KCl | KNO3 |
C | C | CO2 | CO |
D | CuO | Cu | Cu(NO3)2 |
A. AB. BC. CD. D