题目内容
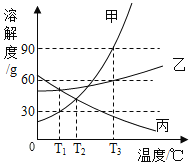
【题目】甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是
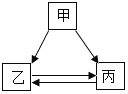
选项 | 甲 | 乙 | 丙 |
A | H2O2 | O2 | H2O |
B | KOH | KCl | KNO3 |
C | C | CO2 | CO |
D | CuO | Cu | Cu(NO3)2 |
A. AB. BC. CD. D
【答案】B
【解析】
A、过氧化氢能生成水和氧气,氧气和水能相互转化,不符合题意;
B、氢氧化钾分别与稀盐酸、稀硝酸反应能生成氯化钾和硝酸钾,氯化钾和硝酸银反应能生成氯化银沉淀和硝酸钾,硝酸钾不能生成氯化钾,符合题意。
C、碳能生成二氧化碳和一氧化碳,一氧化碳和二氧化碳能相互转化,不符合题意;
D、氧化铜能生成铜和硝酸铜,铜和浓硝酸反应生成硝酸铜,硝酸铜和铁等活泼金属反应生成铜单质,能相互转化,不符合题意。故选B。

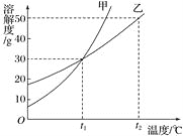
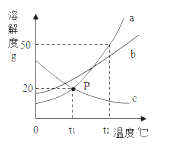
【题目】依据下列实验数据和溶解度曲线完成下面小题。
① | ② | ③ | ④ | |
温度 | 10℃ | 10℃ | 30℃ | 30℃ |
固体种类 | KNO3 | NaCl | KNO3 | NaCl |
固体质量 | 30g | 30g | 40g | 40g |
水的质量 | 100g | 100g | 100g | 100g |
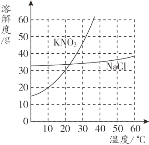
【1】①~④所得的溶液中,属于饱和溶液的是
A. ①和②B. ②和③C. ③和④D. ①和④
【2】下列说法中,正确的是
A. 溶质质量:①=②B. 溶液质量:②>③
C. 溶质质量分数:③>④D. 溶质与溶剂质量比:①=③
【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.

提出问题:久置固体的成分是什么?
查阅资料:铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
作出猜想:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
实验探究:
甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
取少量固体放于试管中,滴加足量的_____. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有_____, 一定不含Fe2O3. |
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是_____.并设计如下实验方案继续验证.
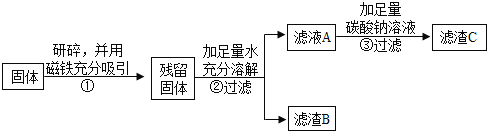
(1)②中固体溶解时放出大量热,由此可以判断固体中一定含有_____.
(2)③中反应的化学方程式是_____.
乙同学对滤渣B又进行探究.
实验操作 | 实验现象 | 实验结论 |
_____ | _____ | 固体中一定含有CaCO3 和Fe2O3. |
丙同学认为乙同学的方案中仍有一种物质不能确定.丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
综合上述实验及所给数据,久置固体的成分是_____.
【题目】焙制糕点所用的发酵粉的主要成分之一是碳酸氢钠,某化学兴趣小组同学对碳酸氢钠的性质进行了以下探究,请回答:
(1)碳酸氢钠俗称___,是生活中一种常见的盐类物质
(2)探究碳酸氢钠溶液的酸碱性
(实验步骤)室温时,取少量碳酸氢钠固体加入试管中,加适量水溶解,用玻璃棒蘸取该溶液滴在pH试纸上,测得该溶液的pH=10。
(实验结论)碳酸氢钠溶液呈___(选填“酸性”碱性或“中性”)。
(3)探究碳酸氢钠固体与酸的反应
(实验步骤)取少量碳酸氢钠固体加入试管中,滴加稀盐酸,有____产生
(实验结论)碳酸氢钠与稀盐酸反应的化学方程式为____
(4)探究碳酸氢钠固体的热稳定性
(查阅资料)碳酸氢钠固体受热易分解,生成水、二氧化碳和一种常见的白色固体物质。
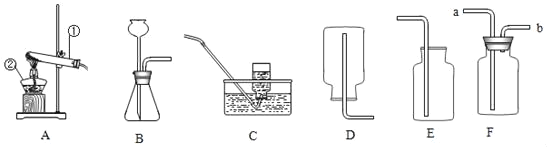
(实验步骤)实验装置如图,充分加热后,试管口有水珠出现,澄清石灰水变浑浊,试管中留下白色固体
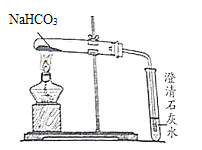
(提出猜想)该兴趣小组的同学认为充分加热后的固体产物可是NaOH或Na2CO3
①他们猜想的依据是___
②请设计实验,检验反应后的固体产物是NaOH或Na2CO3,并完成下表限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管。
序号 | 实验操作 | 预期现象 | 结论 |
Ⅰ | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,加入足量___,振荡,静止 | 产生白色沉淀 | 产物含Na2CO3 |
Ⅱ | 取Ⅰ操作后的上层清液于试管B中,滴加酚酞溶液 | ____ | 产物不含NaOH |
(实验结论)请写出碳酸氢钠受热发生反应的化学方程式:_____
(5)写出碳酸氢钠在生活中的一种用途______