题目内容
【题目】甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )
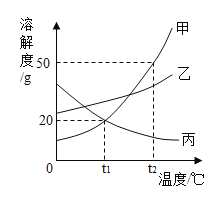
A. t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是:乙>甲=丙
B. t2℃时,30g甲物质加入50g水中,充分搅拌后,所得溶液的溶质的质量分数为37.5%
C. 将相同质量的甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃,析出晶体最多的是甲
D. 欲将丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法
【答案】B
【解析】
A、通过分析溶解度曲线可知,t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是:乙>甲=丙,故A正确;B、t2℃时,甲物质的溶解度是50g,所以30g甲物质加入50g水中,充分搅拌后,所得溶液的溶质的质量分数为![]() ×100%=33.3%,故B错误;C、将相同质量的甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃,甲物质的溶解度变化最大,所以析出晶体最多的是甲,故C正确;D、丙物质的溶解度随温度的升高而减小,所以欲将丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法,故D正确。故选B。
×100%=33.3%,故B错误;C、将相同质量的甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃,甲物质的溶解度变化最大,所以析出晶体最多的是甲,故C正确;D、丙物质的溶解度随温度的升高而减小,所以欲将丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法,故D正确。故选B。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:
【实验探究一】:
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | 猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入 |
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 。
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为 。
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 碱性氧化物(填“是”或“不是”)。