题目内容
【题目】科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图所示)。
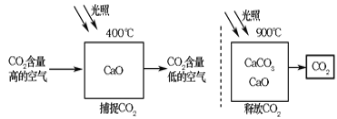
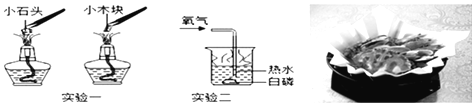
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理是否可行。
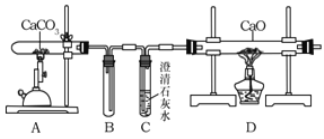
(1)能证明装置A“释放CO2”的现象是_____;
(2)装置B在实验结束撤掉酒精喷灯时的作用是_____;
(3)上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
(猜想与假设)
D中的固体可能为:I.只有氧化钙;Ⅱ._____;Ⅲ.只有碳酸钙
(进行实验)
①甲同学从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。乙同学认为上述实验不足以证明猜想Ⅲ成立,其原因是_____。
②乙同学从D中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是_____。
③丙同学认为乙同学的实验不够严谨,于是向白色固体中加入稀盐酸,再结合乙同学的结论完成下面的实验报告后,除猜想Ⅱ成立的结论。
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | 猜想Ⅱ成立 |
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有_____。
A 原料易得 B 充分利用太阳能 C 释放出的CO2可作为资源加以利用
【答案】C中澄清的石灰水变浑浊 防止C中澄清的石灰水倒吸入A中,使A中热的试管炸裂 氧化钙和碳酸钙 氧化钙与水反应生成的氢氧化钙微溶于水,也可能出现白色不溶物 加入稀盐酸的量少,稀盐酸与氢氧化钙反应,即使有碳酸钙也不会有气泡产生 取一定量的固体于试管中,加水振荡,触摸试管外壁;再向试管中加入足量的稀盐酸 外壁发热;有气泡产生 ABC
【解析】
(1)A、B、C三个装置相连,二氧化碳能使澄清的石灰水变浑浊,故有二氧化碳产生的现象是:C中澄清的石灰水变浑浊。
(2)实验结束撤掉酒精喷灯时,温度降低,装置内压强减小,澄清的石灰水会倒吸入试管,使试管炸裂,有了B装置,澄清的石灰水就不会进入装置A中,故填:防止C中澄清的石灰水倒吸入A中,使A中热的试管炸裂。
(3)D中的固体是氧化钙,氧化钙在高温条件下与二氧化碳反应生成碳酸钙,如果没有反应,固体是氧化钙;如果部分反应,固体是氧化钙、碳酸钙;如果全部反应,固体是碳酸钙,故填:氧化钙和碳酸钙。
①从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物,氧化钙与水反应生成的氢氧化钙微溶于水,也可能产生白色沉淀。
②从D中取一定量的固体于试管中,加入一定量的水,氧化钙与水反应生成氢氧化钙,滴加几滴稀盐酸,氢氧化钙能与稀盐酸反应,稀盐酸的量少,可能只与氢氧化钙反应,也不会有气泡产生,所以该实验不足以证明猜想I成立,故填:加入稀盐酸的量少,稀盐酸与氢氧化钙反应,即使有碳酸钙也不会有气泡产生。
③要通过实验证明猜想Ⅱ成立的实验,猜想Ⅱ中的固体是:氧化钙、碳酸钙。向白色固体中中加入水,触摸试管的外壁,感觉发热,证明白色固体中含有氧化钙;再向剩余固体中滴加足量的稀盐酸,有气泡产生,证明白色固体中含有碳酸钙。故填:
实验步骤 | 实验现象 | 实验结论 |
①取一定量的固体于试管中,加水振荡,触摸试管外壁 ②再向试管中加入足量的稀盐酸 | 外壁发热 有气泡产生 | 猜想Ⅱ成立 |
(4)该设想用二氧化碳和氧化钙在光照的条件下反应,二氧化碳容易得到,释放出的二氧化碳又可以利用,故选:ABC

【题目】我校化学兴趣小组同学为了测定当地石灰石中碳酸钙的质量分数,他们采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(杂质不和盐酸反应,也不溶与水),请帮他们计算:
序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第1次 | 20 | 11 |
第2次 | 20 | 6 |
第3次 | 20 | 2.8 |
第4次 | 20 | n |
(1)碳酸钙的相对分子质量 _______。
(2)上表中n的数值是 _________ 。
(3)样品中碳酸钙的质量分数 _________ 。
(4)生成二氧化碳的质量为__________(写出计算过程)。