题目内容
【题目】实验是学习化学的重要方法。
(实验一)“吹气球实验”如图;
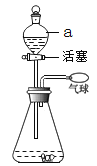
(1)打开活塞,通过仪器a向锥形瓶中加水,观察到气球胀大;关闭活塞,一段时间内气球大小没有变化,说明该装置气密性_______。
(2)若生成氧气使气球胀大,则反应的化学方程式为_______。
(3)若锥形瓶中装有氢氧化钠固体,通过仪器a加少量水,气球也能胀大,主要原因是____。
(实验二)探究酸和碱的性质
(1)电解水时常加入NaOH增强水的导电性,是由于NaOH在水中能解离出______(写粒子符号)。
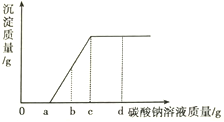
(2)下图为稀硫酸与氢氧化钠溶液反应过程中溶液pH随加入液体体积变化曲线。

①测定溶液pH的方法是:用玻璃棒蘸取溶液,滴到pH试纸上,把试纸显示的颜色与_____对照,读取pH。图2中a点对应的溶液呈______性,若向溶液中加入____,溶液变为红色,也能得出此结论。
②曲线上的b点说明两溶液恰好完全反应,反应的化学方程式为_______。
(3)如图,用注射器吸收液体和CO2(体积比均为1︰5),然后夹紧弹簧夹,用力振荡。
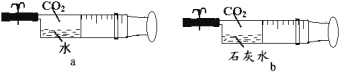

①依据______(填“a、b或c”)现象的对比,可认为氢氧化钠和二氧化碳发生反应,写出该反应的化学方程式______。
②若要证明a中也发生了化学反应,你的实验方案是(写出操作、现象)______。
【答案】 良好 2H2O2![]() 2H2O +O2↑ 氢氧化钠固体溶解时放热 Na+和OH- 标准比色卡 碱 酚酞 2NaOH+H2SO4=Na2SO4+2H2O ac 2NaOH+CO2=Na2CO3+H2O 取少量a中液体滴加石蕊试液,变红色
2H2O +O2↑ 氢氧化钠固体溶解时放热 Na+和OH- 标准比色卡 碱 酚酞 2NaOH+H2SO4=Na2SO4+2H2O ac 2NaOH+CO2=Na2CO3+H2O 取少量a中液体滴加石蕊试液,变红色
【解析】本题考查了检查装置的气密性,实验室制取氧气的反应原理,溶解时的吸热或放热现象,酸和碱的性质。难度不大,根据已有的知识进行分析解答。
实验一:(1)打开活塞,通过仪器a向锥形瓶中加水,观察到气球胀大;关闭活塞,一段时间内气球大小没有变化,说明该装置气密性良好;
(2)该装置是固—液在常温下制取气体的装置,若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是催化剂二氧化锰,倒入的液体是过氧化氢溶液,过氧化氢与二氧化锰混合反应生水和氧气,反应的化学方程式为2H2O2![]() 2H2O +O2↑;
2H2O +O2↑;
(3)氢氧化钠固体溶于水放热。若锥形瓶中装有氢氧化钠固体,通过仪器a加少量水,气球也能胀大,主要原因是氢氧化钠固体溶解时放热。
实验二:(1)氢氧化钠固体溶于水能离解出钠离子和氢氧根离子,符号分别是Na+和OH-;
(2)①测定溶液pH的方法是:用玻璃棒蘸取溶液,滴到pH试纸上,把试纸显示的颜色与比色卡对照,读取pH。图2中a点对应的溶液pH大于 7,溶液呈碱性,酚酞溶液遇碱性溶液呈红色,若向溶液中加入酚酞溶液,溶液变为红色,也能得出此结论。
②氢氧化钠与硫酸反应生成硫酸钠和水,反应的化学方程式是2NaOH+H2SO4=Na2SO4+2H2O;
(3)①a中二氧化碳与水混合,c中二氧化碳与氢氧溶液混合,水和氢氧化钠溶液的体积相同,依据ac现象的对比可认为氢氧化钠和二氧化碳发生反应,氢氧化钠与二氧化碳反应生成碳酸钠和水,反应的化学方程式是2NaOH+CO2=Na2CO3+H2O;
②二氧化碳与水反应生成碳酸,碳酸呈酸性,能使石蕊溶液变红色,可用石蕊溶液检验a中是否发生化学反应。实验方案是取少量a中液体滴加石蕊试液,变红色。

 黄冈创优卷系列答案
黄冈创优卷系列答案