题目内容
【题目】根据要求回答问题。
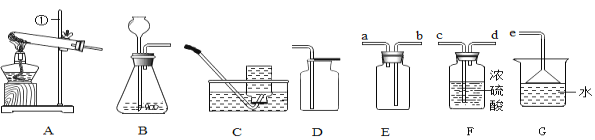
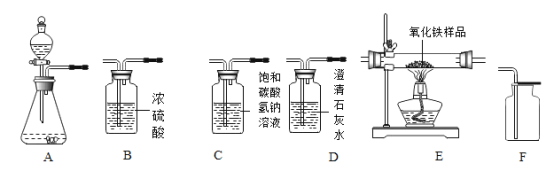
(1)写出仪器①的名称_______。
(2)用氯酸钾和二氧化锰制取氧气的化学方程式为______,该反应属于______。(填基本反应类型)用装置C收得的氧气不纯,可能的原因是______。若用装置A装高锰酸钾制取氧气,则装置需要补充____。若要收集到较纯净的氧气,其收集装置应选__(填字母)。
(3)用向上排空气法收集到的气体,检验是否为氧气的操作是____。
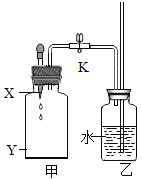
(4)通常状态下,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水形成盐酸。用如图所示装置收集一瓶干燥的HCl,装置的导管按气流方向连接的顺序是:气体→_→_____→_____→_____→e(填字母)。
(5)G装置烧杯中的水改成氢氧化钠溶液可吸收污染物五氧化二磷,生成磷酸钠(Na3PO4)和水,反应的化学方程式为______。
(6)为了探究气体氨气(NH3) 的某些性质,小雨同学查阅了有关资料,知道具有碱性的物质可以使无色酚酞溶液变红;然后依次做了以下实验。
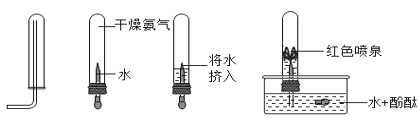
由以上实验,得出氨气的物理性质有_____________、_____________。
【答案】铁架台 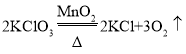 分解反应 未等气泡连续均匀冒出时就开始收集气体。(合理就给分) 在试管口塞一团棉花 C 将带火星的木条伸入集气瓶内,木条复燃,证明该气体是氧气 c d b a
分解反应 未等气泡连续均匀冒出时就开始收集气体。(合理就给分) 在试管口塞一团棉花 C 将带火星的木条伸入集气瓶内,木条复燃,证明该气体是氧气 c d b a ![]() 密度比空气小 极易溶于水
密度比空气小 极易溶于水
【解析】
(1)由图可知,仪器①的名称是铁架台,故填铁架台。
(2)氯酸钾在二氧化锰作催化剂和加热的条件下反应生成氯化钾和氧气,故反应的化学方程式写为:2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
由化学方程式可知,该反应是一种物质反应生成两种新物质的反应,属于分解反应,故填分解反应;
用排水法收集气体后得到的气体不纯净,可能的原因是未等气泡连续均匀冒出时就开始收集气体,收集的气体中混有空气,使气体不纯净,故填未等气泡连续均匀冒出时就开始收集气体;
加热高锰酸钾制取氧气时,为避免高锰酸钾颗粒进入导管,应在装置A试管口处放一团棉花,故填在试管口塞一团棉花;
氧气不易溶于水,收集纯净的氧气可选择排水法,即装置C,故填C。
(3)氧气具有助燃性,能够使带火星的木条复燃,所以检验气体是否为氧气的操作是将带火星的木条伸入集气瓶内,木条复燃,证明该气体是氧气,故填将带火星的木条伸入集气瓶内,木条复燃,证明该气体是氧气。
(4)为得到干燥的HCl气体,先将HCl气体沿装置F的长管,即c管通入浓硫酸中进行干燥,再沿短管,即d管排出,HCl气体的密度大于空气的密度,所以从d管导出的气体再沿装置E的长管,即b管进入装置E进行收集,收集满HCl气体后,多余的HCl气体再沿a管排出进入e管被水吸收,防止HCl气体污染空气,所以导管按气流方向连接的顺序是cdbae,故填cdba。
(5)五氧化二磷是一种非金属氧化物,所以氢氧化钠与五氧化二磷反应生成磷酸钠和水,故反应的化学方程式写为:P2O5+6NaOH=2Na3PO4+3H2O。
(6)由图可知,收集氨气采用向上排空气法,说明氨气的密度比空气的密度小,向干燥的氨气中挤入少量水后,装置中形成喷泉,说明氨气极易溶于水,物质的密度与溶解性都属于物理性质,故填密度比空气小和极易溶于水。

【题目】宏宏发现氢氧化钠溶液忘记盖瓶盖。对于该溶液是否变质,宏宏等同学进行了探究。请你一起完成下列实验报告。
(1) [提出问题1]该溶液是否变质?
[实验探究1]
实验步骤 | 实验现象 | 解释与结论 |
取少量该溶液放于试管中,滴加足量稀盐酸 | 有_________产生 | 说明该溶液已变质。变质的原因是_______(请用化学方程式表示)。 |
(2) [提出问题2]该溶液变质程度怎样?
[提出猜想]
猜想一:已完全变质,该溶液中溶质只含Na2CO3
猜想二:部分变质,该溶液中溶质含有___________。
[查阅资料]氯化钡溶液呈中性。
[实验探究2]
实验步骤 | 实验现象 | 结论 |
先取少量该溶液放于试管中,加入过量氯化钡溶液 | 有________生成 | 猜想__________成立 |
静置,取上层清液于另一支试管中,加入2- 3滴酚酞溶液 | 上层清液变红 |
(3) [提出问题3]怎样提纯该样品得到纯净的氢氧化钠固体。
[实验探究3]为得到纯净的氢氧化钠固体,同学们取该样品并设计了如图实验方案。
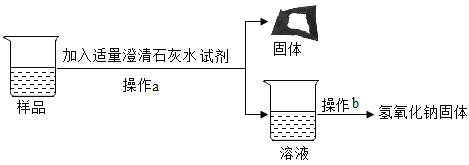
请回答下列问题:
①操作a和操作b中都需用到玻璃棒,其中操作a中玻璃棒的作用为_____________.
②根据实验流程可知,最终所得氢氧化钠固体质量___________变质后样品中氢氧化钠的质量(填“大于”、“小于”或“等于”)。
(4)[反思交流]在[实验探究2]中加入过量的氯化钡溶液的目的是_____________.
(5) [拓展提升]宏宏在完成实验室制取CO2后,对回收的盐酸和CaCl2混合溶液(不考虑其它杂质)进行以下实验:取200g该溶液于烧杯中,向其中滴加溶质质量分数为10. 6%的Na2CO3溶液,滴入Na2CO3溶液与生成沉淀的质量关系如图所示。
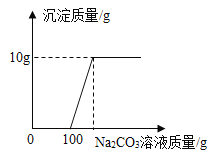
①回收液中HCl的质量分数是多少?___ (写出计算过程)
②当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量是多少g?___(写出计算过程)