��Ŀ����
����Ŀ��AgNO3�����ڵ�Ӱ��Ƭ��������ȡ����NaNO3��AgNO3��Ʒ100g����һ������������Ʒ��ַ�Ӧ��ֻ��AgNO3������Ӧ���õ�����69g���ù����з�����Ӧ�Ļ�ѧ����ʽΪ:2AgNO3 2Ag+2NO2��+O2�����Լ���:
2Ag+2NO2��+O2�����Լ���:
(1)AgNO3��N��OԪ�ص�������Ϊ_____��
(2)�ֽ�����Ļ��������O2��������_____
(3)��ȡ100g����Ʒ��һ��������NaCl����ȫ���ܽ���142.5gˮ�еõ���һ�����ʵ���Һ������Һ���ʵ����������Ƕ���?_____
���𰸡�7��24 8g 33.7%
��������
��1��AgNO3��N��OԪ�ص�������Ϊ14:16��3=7��24��
��2��������������Ϊx���ֽ�����Ļ��������O2������Ϊy��������������Ϊ69g-��100g-x��=x-31g;
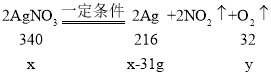
![]()
x=85g,y=8g
�𣺷ֽ�����Ļ��������O2������Ϊ8g��
��3����85g��������ȫ��Ӧ���ɳ���������Ϊm�����������Ƶ�����Ϊn��

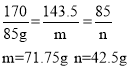
��Һ��Һ���ʵ���������Ϊ��![]()
�𣺸���Һ���ʵ�����������33.7%��

��ϰ��ϵ�д�
 ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д� ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
�����Ŀ