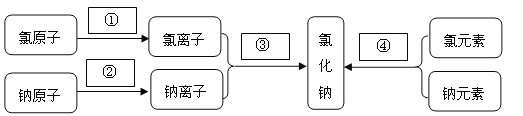
题目内容
【题目】 如图四个图象中能正确反应其对应实验操作的是
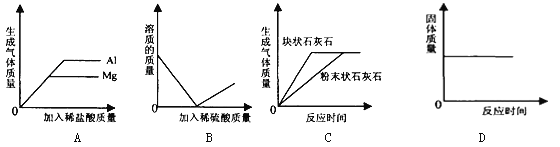
A.向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸
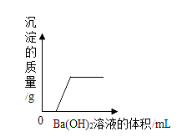
B.向一定量的氢氧化钡溶液中不断加入稀硫酸
C.等质量的块状石灰石和粉末状石灰石分别与质量分数相同的足量的稀盐酸反应
D.碳和氧化铜的固体混合物在高温条件下反应
【答案】AB
【解析】
试题分析:解答图像类的题目抓住“三点一走势”,即首先看清楚横、纵坐标各表示的量,然后从起始点、转折点、终点还有量的变化趋势来进行分析解答,A、向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸,由于横坐标表示的是加入稀盐酸的量,故刚开始产生的氢气质量相等,但最终Al消耗的盐酸更多,产生的氢气质量更大,正确,B、向一定量的氢氧化钡溶液中不断加入稀硫酸,由于反应生成硫酸钡沉淀,故随着稀硫酸的不断加入,溶液质量不断减少,当氢氧化钡溶液完全被消耗完,溶质质量变为0,然后稀硫酸过量,故溶质质量又开始增大,正确,C、等质量的块状石灰石和粉末状石灰石分别与质量分数相同的足量的稀盐酸反应,反应物的接触面积越大,反应速率就越快,故粉末状石灰石与稀盐酸反应的速率更快,错误,D、碳和氧化铜的固体混合物在高温条件下反应,由于反应生成二氧化气体,故固体质量应不断减少,直至反应结束,不再发生变化,错误,故选AB

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室有一瓶长期露置于空气中氢氧化钠溶液,确认已变质。某学习小组展开如下探究,确定该溶液的成分,并进一步制定回收方案。
【问题1】久置的氢氧化钠溶液是全部变质?还是部分变质?
【探究1】确定该溶液中溶质的成分。
【资料1】BaCl2溶液、Ba(NO3)2溶液、CaCl2溶液、Ca(NO3)2溶液、NaNO3溶液均显中性。
实验操作 | 实验现象 | 实验结论 |
Ⅰ.取少量溶液于试管中,向溶液中滴加 (14) 溶液,并不断振荡。 | 白色沉淀产生 | 该溶液部分变质,含有 碳酸钠和氢氧化钠。 |
Ⅱ.将步骤Ⅰ反应后的混合物静置,取少量上层清液,滴加2~3滴酚酞试液。 | (15) |
氢氧化钠溶液变质的原因 (16) (用化学方程式表示),因此氢氧化钠溶液必须密封保存。
【问题2】如何从变质的氢氧化钠溶液中回收得到较纯净的氢氧化钠固体。
【探究2】回收纯净的氢氧化钠固体。
【资料2】在不同温度下NaOH的溶解度如下:
温度(℃) | 10 | 20 | 40 | 60 | 80 | 100 |
溶解度(g/100g水) | 64 | 85 | 138 | 203 | 285 | 376 |
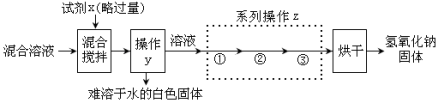
请回答下列问题:
Ⅰ.试剂x的化学式 (17) ,操作y的名称为 (18) 。
Ⅱ.根据相关物质的溶解度数据,系列操作z中 ② 操作名称为 (19) 。
Ⅲ.探究1中的物质检验和探究2中的除杂提纯都将碳酸钠进行了转化,但二者目的不同,分别是 (20) 、 (21) 。